Page 76 - E-modul Struktur Atom-Keunggulan Nanoteknologi 2023 Untuk Guru
P. 76
Tabel Periodik Modern (Moseley)
Tabel periodik modern didasarkan pada Hukum Periodik Moseley. Henry Moseley
mengusulkan untuk menyusun unsur-unsur berdasarkan kenaikan nomor atom. Ketika atom
disusun berdasarkan kenaikan nomor atomnya, kelemahan tabel periodik Mendeleev
menghilang. Moseley merevisi tabel periodik dan membuat perubahan dengan menyusun
unsur berdasarkan kenaikan nomor atomnya dengan melakukan perubahan ini, Moseley
menekankan pada konfigurasi elektron unsur yang menentukan sifat fisika dan kimia suatu
unsur. Dalam tabel periodik modern, atom-atom dengan konfigurasi elektron yang sama
ditempatkan pada kolom yang sama. Kolom disebut golongan, sedangkan unsur-unsur dalam
periode menunjukkan peningkatan integral dalam elektron valensi. Kolom ini disebut periode.
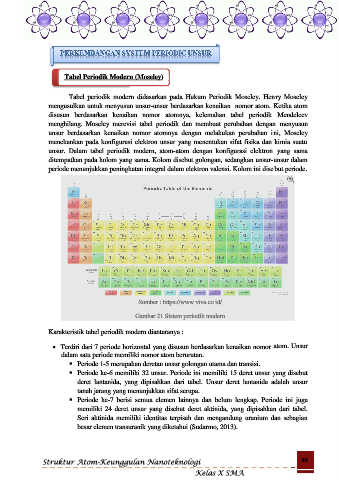
Sumber : https://www.viva.co.id/
Gambar 21 Sistem periodik modern
Karakteristik tabel periodik modern diantaranya :
Terdiri dari 7 periode horizontal yang disusun berdasarkan kenaikan nomor atom. Unsur
dalam satu periode memiliki nomor atom berurutan.
Periode 1-5 merupakan deretan unsur golongan utama dan transisi.
Periode ke-6 memiliki 32 unsur. Periode ini memiliki 15 deret unsur yang disebut
deret lantanida, yang dipisahkan dari tabel. Unsur deret lantanida adalah unsur
tanah jarang yang menunjukkan sifat serupa.
Periode ke-7 berisi semua elemen lainnya dan belum lengkap. Periode ini juga
memiliki 24 deret unsur yang disebut deret aktinida, yang dipisahkan dari tabel.
Seri aktinida memiliki identitas terpisah dan mengandung uranium dan sebagian
besar elemen transuranik yang diketahui (Sudarmo, 2013).
Struktur Atom-Keunggulan Nanoteknologi 43
Kelas X SMA