Page 34 - E-BOOK SIAP MASUK FLIP PDF PRO_Neat
P. 34
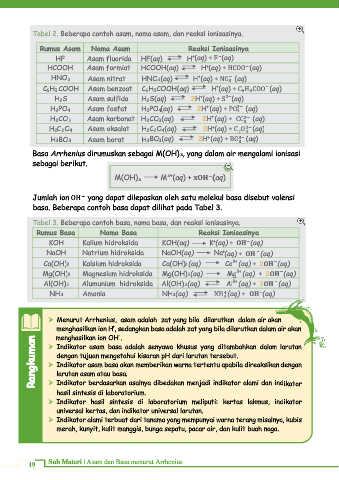
Tabel 2. Beberapa contoh asam, nama asam, dan reaksi ionisasinya.
Rumus Asam Nama Asam Reaksi Ionisasinya
HF Asam fluorida HF(aq) H (aq) + F (aq)
+
−
+
HCOOH Asam formiat HCOOH(aq) H (aq) + HCOO (aq)
−
+
HNO3 Asam nitrat HNO3(aq) H (aq) + NO (aq)
−
3
C6H5COOH Asam benzoat C6H5COOH(aq) H (aq) + C H COO (aq)
+
−
5
6
H2S Asam sulfida H2S(aq) 2H (aq) + S (aq)
+
2−
+
H2PO4 Asam fosfat H2PO4(aq) 2H (aq) + PO (aq)
2−
4
+
H2CO3 Asam karbonat H2CO3(aq) 2H (aq) + CO (aq)
2−
3
+
2−
H2C2O4 Asam oksalat H2C2O4(aq) 2H (aq) + C O (aq)
2 4
+
3−
H3BO3 Asam borat H3BO3(aq) 3H (aq) + BO (aq)
3
Basa Arrhenius dirumuskan sebagai M(OH)x, yang dalam air mengalami ionisasi
sebagai berikut.
M(OH)x M (aq) + (aq)
x+
−
Jumlah ion OH yang dapat dilepaskan oleh satu molekul basa disebut valensi
−
basa. Beberapa contoh basa dapat dilihat pada Tabel 3.
Tabel 3. Beberapa contoh basa, nama basa, dan reaksi ionisasinya.
Rumus Basa Nama Basa Reaksi Ionisasinya
KOH Kalium hidroksida KOH(aq) K (aq) + (aq)
+
−
+
NaOH Natrium hidroksida NaOH(aq) Na (aq) + (aq)
−
2+
−
Ca(OH)2 Kalsium hidroksida Ca(OH)2(aq) Ca (aq) + (aq)
2+
Mg(OH)2 Magnesium hidroksida Mg(OH)2(aq) Mg (aq) + (aq)
−
Al(OH)3 Alumunium hidroksida Al(OH)3(aq) Al (aq) + (aq)
2+
−
−
+
NH3 Amonia NH3(aq) NH (aq) + (aq)
4
Menurut Arrhenius, asam adalah zat yang bila dilarutkan dalam air akan
+
menghasilkan ion H , sedangkan basa adalah zat yang bila dilarutkan dalam air akan
menghasilkan ion OH .
-
Indikator asam basa adalah senyawa khusus yang ditambahkan dalam larutan
dengan tujuan mengetahui kisaran pH dari larutan tersebut.
Indikator asam basa akan memberikan warna tertentu apabila direaksikan dengan
larutan asam atau basa.
Rangkuman Indikator berdasarkan asalnya dibedakan menjadi indikator alami dan indikator
hasil sintesis di laboratorium.
Indikator hasil sintesis di laboratorium meliputi: kertas lakmus, indikator
universal kertas, dan indikator universal larutan.
Indikator alami terbuat dari tanama yang mempunyai warna terang misalnya, kubis
merah, kunyit, kulit manggis, bunga sepatu, pacar air, dan kulit buah naga.
19 Sub Materi | Asam dan Basa menurut Arrhenius