Page 21 - E-MODUL AR
P. 21
Setelah mengetahui tentang teori VSEPR dan teori domain elektron maka kita
dapat meramalkan bentuk geometri suatu molekul, seperti terlihat pada gambar
dan penjelasan berikut:
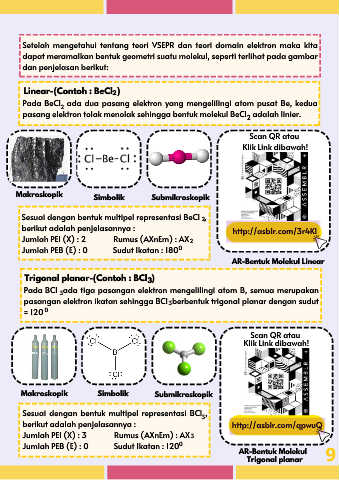
Linear-(Contoh : BeCl )
2
Pada BeCl ada dua pasang elektron yang mengelilingi atom pusat Be, kedua
2
pasang elektron tolak menolak sehingga bentuk molekul BeCl adalah linier.
2
Scan QR atau
Klik Link dibawah!
Makroskopik Simbolik Submikroskopik
Sesuai dengan bentuk multipel representasi BeCl ,
2
berikut adalah penjelasannya : http://asblr.com/3r4Kl
Jumlah PEI (X) : 2 Rumus (AXnEm) : AX 2
Jumlah PEB (E) : 0 Sudut Ikatan : 180 0
AR-Bentuk Molekul Linear
Trigonal planar-(Contoh : BCl )
3
Pada BCl ada tiga pasangan elektron mengelilingi atom B, semua merupakan
3
pasangan elektron ikatan sehingga BCl berbentuk trigonal planar dengan sudut
3
= 120 0
Scan QR atau
Klik Link dibawah!
Makroskopik Simbolik Submikroskopik
Sesuai dengan bentuk multipel representasi BCl ,
3
berikut adalah penjelasannya : http://asblr.com/qpwuQ
Jumlah PEI (X) : 3 Rumus (AXnEm) : AX3
Jumlah PEB (E) : 0 Sudut Ikatan : 120 0
AR-Bentuk Molekul 9
Trigonal planar