Page 22 - Draft Bahan Ajar BF
P. 22
REAKSI
REDUKSI OKSIDASI
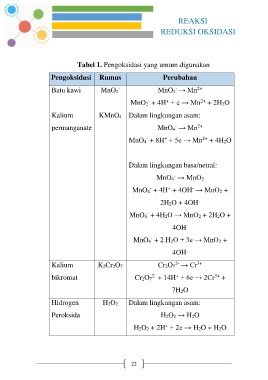
Tabel 1. Pengoksidasi yang umum digunakan
Pengoksidasi Rumus Perubahan
-
-
Batu kawi MnO2 MnO2 → Mn 2+
-
+
2+
MnO2 + 4H + e → Mn + 2H2O
Kalium KMnO4 Dalam lingkungan asam:
-
permanganate MnO4 → Mn 2+
-
+
2+
MnO4 + 8H + 5e → Mn + 4H2O
Dalam lingkungan basa/netral:
-
MnO4 → MnO2
-
+
-
MnO4 + 4H + 4OH → MnO2 +
2H2O + 4OH -
-
MnO4 + 4H2O → MnO2 + 2H2O +
4OH -
MnO4 + 2 H2O + 3e → MnO2 +
-
-
4OH
2-
Kalium K2Cr2O7 Cr2O7 → Cr 3+
+
3+
2-
bikromat Cr2O7 + 14H + 6e → 2Cr +
7H2O
Hidrogen H2O2 Dalam lingkungan asam:
Peroksida H2O2 → H2O
H2O2 + 2H + 2e → H2O + H2O
+
22