Page 44 - Kesetimbangan Kimia ref 12_Neat
P. 44
E-MODUL KIMIA
BERBASIS INTEGRATED GUIDED INQUIRY (IGI)
konsentrasi zat-zat yang berada dalam kesetimbangan.
Hubungan ini dikenal dengan Hukum Kesetimbangan
Kimia atau Hukum Aksi Massa. Menurut Hukum Aksi
Massa,
“Untuk reaksi kimia pada suhu tertentu, perbandingan
hasil kali konsentrasi zat-zat di ruas kanan dengan hasil
kali konsentrasi zat-zat di ruas kiri, yang masing-masing
dipangkatkan dengan koefisien reaksinya, akan
menghasilkan suatu bilangan yang tetap (konstan)”
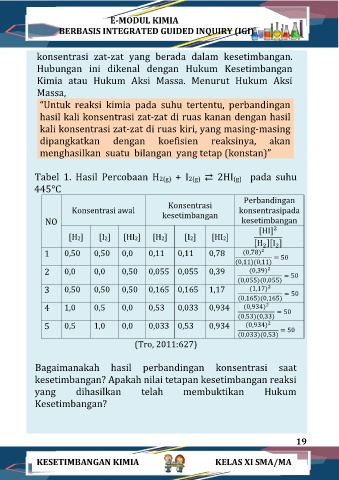
Tabel 1. Hasil Percobaan H2(g) + I2(g) ⇄ 2HI(g) pada suhu
445°C
Perbandingan
Konsentrasi
Konsentrasi awal kesetimbangan konsentrasipada
NO kesetimbangan
[H2] [I2] [HI2] [H2] [I2] [HI2]
1 0,50 0,50 0,0 0,11 0,11 0,78
2 0,0 0,0 0,50 0,055 0,055 0,39
3 0,50 0,50 0,50 0,165 0,165 1,17
4 1,0 0,5 0,0 0,53 0,033 0,934
5 0,5 1,0 0,0 0,033 0,53 0,934
(Tro, 2011:627)
Bagaimanakah hasil perbandingan konsentrasi saat
kesetimbangan? Apakah nilai tetapan kesetimbangan reaksi
yang dihasilkan telah membuktikan Hukum
Kesetimbangan?
19
KESETIMBANGAN KIMIA KELAS XI SMA/MA