Page 4 - التحليل الكيميائي ahmed
P. 4
4
ﺍﻟﻜﺸﻒ ﻋﻦ ﺍﻟﺸﻘﻮﻕ ﺍﳊﺎﻣﻀﻴﺔ)ﺍﻻﻧﻴﻮﻧﺎﺕ(:
ﺗﻨﻘﺴﻢ اﻻﻧﯿﻮﻧﺎت )اﻟﺸﻘﻮق اﻟﺤﺎﻣﻀﯿﺔ( اﻟﻲ ﺛﻼﺛﺔ ﻣﺠﻤﻮﻋﺎت ﻟﻜﻞ ﻣﻨﮭﺎ ﻛﺎﺷﻒ ﻣﻌﯿﻦ وھﻲ:
-1ﻣﺠﻤﻮﻋﺔ اﻧﯿﻮﻧﺎت ﺣﻤﺾ اﻟﮭﯿﺪرﻛﻠﻮرﯾﻚ اﻟﻤﺨﻔﻒ HCLﻣﺨﻔﻒ
-2ﻣﺠﻤﻮﻋﺔ اﻧﯿﻮﻧﺎت ﺣﻤﺾ اﻟﻜﺒﺮﯾﺘﯿﻚ اﻟﻤﺮﻛﺰ H2SO4ﻣﺮﻛﺰ
-3ﻣﺠﻤﻮﻋﺔ اﻧﯿﻮﻧﺎت ﻣﺤﻠﻮل ﻛﻠﻮرﯾﺪ اﻟﺒﺎرﯾﻮم
ﺍﻻﺳﺎﺱ ﺍﻟﻌﻠﻤﻲ ﻟﻠﻜﺸﻒ ﻋﻦ ﺍﻻﻧﻴﻮﻧﺎﺕ)ﺍﻟﺸﻘﻮﻕ ﺍﳊﺎﻣﻀﻴﺔ(:
اﻟﺤﻤﺾ اﻻﻛﺜﺮ ﺛﺒﺎﺗﺎ )اﻻﻗﻞ ﺗﻄﺎﯾﺮا( ﯾﻄﺮد اﻟﺤﻤﺾ اﻻﻗﻞ ﺛﺒﺎﺗﺎ )اﻻﻛﺜﺮ ﺗﻄﺎﯾﺮا واﻧﺤﻼﻻ( ﻣﻦ ﻣﻠﺤﮫ ﻓﻲ ﺻﻮرة ﻏﺎزات ﯾﻤﻜﻦ
اﻟﺘﻌﺮف ﻋﻠﯿﮭﺎ ﺑﺎﻟﻜﺎﺷﻒ اﻟﻤﻨﺎﺳﺐ وﯾﻔﻀﻞ اﻟﺘﺴﺨﯿﻦ اﻟﮭﯿﻦ ﻟﻄﺮد اﻟﻐﺎزات
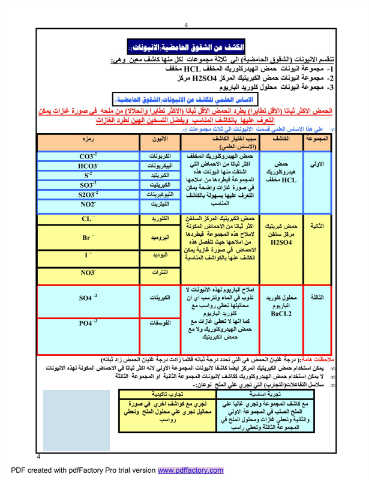
• ﻋﻠﻲ ھﺬا اﻻﺳﺎس اﻟﻌﻠﻤﻲ ﻗﺴﻤﺖ اﻻﻧﯿﻮﻧﺎت اﻟﻲ ﺛﻼث ﻣﺠﻤﻮﻋﺎت -:
رﻣﺰه اﻻﻧﯿﻮن اﻟﻤﺠﻤﻮﻋﺔ اﻟﻜﺎﺷﻒ ﺳﺒﺐ اﺧﺘﯿﺎر اﻟﻜﺎﺷﻒ
)اﻻﺳﺎس اﻟﻌﻠﻤﻲ(
CO3-2 اﻟﻜﺮﺑﻮﻧﺎت ﺣﻤﺾ اﻟﮭﯿﺪروﻛﻠﻮرﯾﻚ اﻟﻤﺨﻔﻒ ﺣﻤﺾ اﻻوﻟﻲ
HCO3- اﻟﺒﯿﻜﺮﺑﻮﻧﺎت اﻛﺜﺮ ﺛﺒﺎﺗﺎ ﻣﻦ اﻻﺣﻤﺎض اﻟﺘﻲ ھﯿﺪروﻛﻠﻮرﯾﻚ
اﻟﻜﺒﺮﯾﺘﯿﺪ HCLﻣﺨﻔﻒ
S-2 اﻟﻜﺒﺮﯾﺘﯿﺖ اﺷﺘﻘﺖ ﻣﻨﮭﺎ اﻧﯿﻮﻧﺎت ھﺬه
SO3-2 اﻟﺜﯿﻮﻛﺒﺮﯾﺘﺎت اﻟﻤﺠﻤﻮﻋﺔ ﻓﯿﻄﺮدھﺎ ﻣﻦ اﻣﻼﺣﮭﺎ
S2O3-2 ﻓﻲ ﺻﻮرة ﻏﺎزات واﺿﺤﺔ ﯾﻤﻜﻦ
اﻟﺘﻌﺮف ﻋﻠﯿﮭﺎ ﺑﺴﮭﻮﻟﺔ ﺑﺎﻟﻜﺎﺷﻒ
NO2- اﻟﻨﯿﺘﺮﯾﺖ اﻟﻤﻨﺎﺳﺐ
ﺣﻤﺾ اﻟﻜﺒﺮﯾﺘﯿﻚ اﻟﻤﺮﻛﺰ اﻟﺴﺎﺧﻦ اﻟﻜﻠﻮرﯾﺪ – CL
اﻟﺜﺎﻧﯿﺔ ﺣﻤﺾ ﻛﺒﺮﯾﺘﯿﻚ اﻛﺜﺮ ﺛﺒﺎﺗﺎ ﻣﻦ اﻻﺣﻤﺎض اﻟﻤﻜﻮﻧﺔ
– Br اﻟﺒﺮوﻣﯿﺪ ﻻﻣﻼح ھﺬه اﻟﻤﺠﻤﻮﻋﺔ ﻓﯿﻄﺮدھﺎ ﻣﺮﻛﺰ ﺳﺎﺧﻦ
ﻣﻦ اﻣﻼﺣﮭﺎ ﺣﯿﺚ ﺗﻨﻔﺼﻞ ھﺬه H2SO4
–I اﻟﯿﻮدﯾﺪ اﻻﺣﻤﺎض ﻓﻲ ﺻﻮرة ﻏﺎزﯾﺔ ﯾﻤﻜﻦ
اﻟﻜﺸﻒ ﻋﻨﮭﺎ ﺑﺎﻟﻜﻮاﺷﻒ اﻟﻤﻨﺎﺳﺒﺔ
NO3- اﻟﻨﺘﺮات
SO4 -2 اﻟﻜﺒﺮﯾﺘﺎت اﻣﻼح اﻟﺒﺎرﯾﻮم ﻟﮭﺬه اﻻﻧﯿﻮﻧﺎت ﻻ ﻣﺤﻠﻮل ﻛﻠﻮرﯾﺪ اﻟﺜﺎﻟﺜﺔ
PO4 -3 اﻟﻔﻮﺳﻔﺎت ﺗﺬوب ﻓﻲ اﻟﻤﺎء وﺗﺘﺮﺳﺐ أي ان اﻟﺒﺎرﯾﻮم
ﻣﺤﺎﻟﯿﻠﮭﺎ ﺗﻌﻄﻲ رواﺳﺐ ﻣﻊ BaCL2
ﻛﻠﻮرﯾﺪ اﻟﺒﺎرﯾﻮم
ﻛﻤﺎ اﻧﮭﺎ ﻻ ﺗﻌﻄﻲ ﻏﺎزات ﻣﻊ
ﺣﻤﺾ اﻟﮭﯿﺪروﻛﻠﻮرﯾﻚ وﻻ ﻣﻊ
ﺣﻤﺾ اﻟﻜﺒﺮﯾﺘﯿﻚ
ﻣﻼﺣﻈﺎت ھﺎﻣﺔ ):درﺟﺔ ﻏﻠﯿﺎن اﻟﺤﻤﺾ ھﻲ اﻟﺘﻲ ﺗﺤﺪد درﺟﺔ ﺛﺒﺎﺗﮫ ﻓﻜﻠﻤﺎ زادت درﺟﺔ ﻏﻠﯿﺎن اﻟﺤﻤﺾ زاد ﺛﺒﺎﺗﮫ(
• ﯾﻤﻜﻦ اﺳﺘﺨﺪام ﺣﻤﺾ اﻟﻜﺒﺮﯾﺘﯿﻚ اﻟﻤﺮﻛﺰ اﯾﻀﺎ ﻛﺎﺷﻔﺎ ﻻﻧﯿﻮﻧﺎت اﻟﻤﺠﻤﻮﻋﺔ اﻻوﻟﻲ ﻻﻧﮫ اﻛﺜﺮ ﺛﺒﺎﺗﺎ ﻓﻲ اﻻﺣﻤﺎض اﻟﻤﻜﻮﻧﺔ ﻟﮭﺬه اﻻﻧﯿﻮﻧﺎت
• ﻻ ﯾﻤﻜﻦ اﺳﺘﺨﺪام ﺣﻤﺾ اﻟﮭﯿﺪروﻛﻠﻮرﯾﻚ ﻛﻜﺎﺷﻒ ﻻﻧﯿﻮﻧﺎت اﻟﻤﺠﻤﻮﻋﺔ اﻟﺜﺎﻧﯿﺔ او اﻟﻤﺠﻤﻮﻋﺔ اﻟﺜﺎﻟﺜﺔ
• ﺳﻼﺳﻞ اﻟﺘﻔﺎﻋﻼت)اﻟﺘﺠﺎرب( اﻟﺘﻲ ﺗﺠﺮي ﻋﻠﻲ اﻟﻤﻠﺢ ﻧﻮﻋﺎن-:
ﺗﺠﺎرب ﺗﺎﻛﯿﺪﯾﺔ ﺗﺠﺮﺑﺔ اﺳﺎﺳﯿﺔ
ﺗﺠﺮي ﻣﻊ ﻛﻮاﺷﻒ اﺧﺮي ﻓﻲ ﺻﻮرة ﻣﻊ ﻛﺎﺷﻒ اﻟﻤﺠﻤﻮﻋﺔ وﺗﺠﺮي ﻏﺎﻟﺒﺎ ﻋﻠﻲ
ﻣﺤﺎﻟﯿﻞ ﺗﺠﺮي ﻋﻠﻲ ﻣﺤﻠﻮل اﻟﻤﻠﺢ وﺗﻌﻄﻲ اﻟﻤﻠﺢ اﻟﺼﻠﺐ ﻓﻲ اﻟﻤﺠﻤﻮﻋﺔ اﻻوﻟﻲ
رواﺳﺐ واﻟﺜﺎﻧﯿﺔ وﺗﻌﻄﻲ ﻏﺎزات وﻣﺤﻠﻮل اﻟﻤﻠﺢ ﻓﻲ
اﻟﻤﺠﻤﻮﻋﺔ اﻟﺜﺎﻟﺜﺔ وﺗﻌﻄﻲ راﺳﺐ
4
PDF created with pdfFactory Pro trial version www.pdffactory.com