Page 211 - Buku Kimia Unsur Golongan Utama Berbasis PBL
P. 211
Titik didih dan Titik lebur
Besarnya titik didih suatu zat dipengaruhi oleh jenis / kekuatan ikatan yang dimiliki zat tersebut . Semakin besar masa atom semakin tinggi titik didihnya .hal ini disebabkan karena makin besar masa atom semakin besar pula ikatan Van der waals-nya,sehingga untuk memutuskan ikatan antar molekul ini diperlukan energi yang lebih besar.
Demikian pula dengan titik lebur,semakin besar massa atom gas mulia,semakin kuat ikatan Van der waals-nya,akibat titik lebur semakin tinggi.
Daya hantar listrik dan panas
Logam dapat menghantarkan listrik karena elektron valensinya bebas pindah dari atom satu keatom lainnya. Atom-atom gas mulia tidak menghantarkan listrik dan panas karena elektron valensinya tidak bisa bergerak bebas.
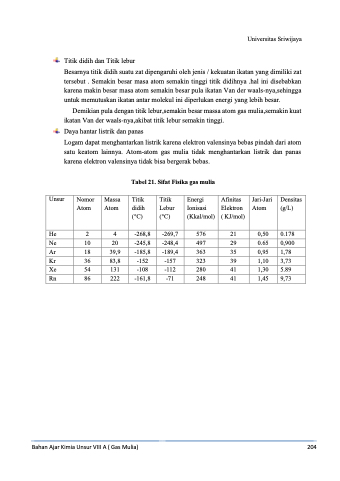
Tabel 21. Sifat Fisika gas mulia
Universitas Sriwijaya
Unsur
Nomor Atom
Massa Atom
Titik didih (°C)
Titik Lebur (°C)
Energi Ionisasi (Kkal/mol)
Afinitas Elektron ( KJ/mol)
Jari-Jari Atom
Densitas (g/L)
He Ne Ar Kr Xe Rn
24 10 20 18 39,9 36 83,8 54 131 86 222
-268,8 -269,7 -245,8 -248,4 -185,8 -189,4 -152 -157 -108 -112 -161,8 -71
576 21 497 29 363 35 323 39 280 41 248 41
0,50 0.178 0.65 0,900 0,95 1,78 1,10 3,73 1,30 5.89 1,45 9,73
Bahan Ajar Kimia Unsur VIII A ( Gas Mulia)
204