Page 23 - Kimia Fisika
P. 23
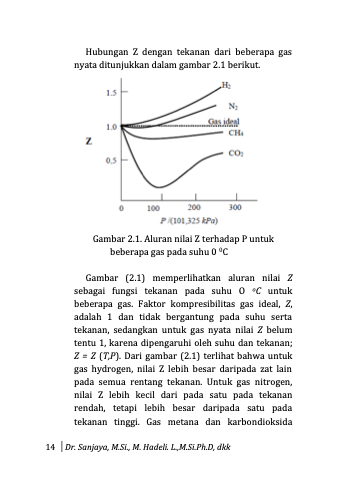
Hubungan Z dengan tekanan dari beberapa gas nyata ditunjukkan dalam gambar 2.1 berikut.
Gambar 2.1. Aluran nilai Z terhadap P untuk beberapa gas pada suhu 0 0C
Gambar (2.1) memperlihatkan aluran nilai Z sebagai fungsi tekanan pada suhu O oC untuk beberapa gas. Faktor kompresibilitas gas ideal, Z, adalah 1 dan tidak bergantung pada suhu serta tekanan, sedangkan untuk gas nyata nilai Z belum tentu 1, karena dipengaruhi oleh suhu dan tekanan; Z = Z (T,P). Dari gambar (2.1) terlihat bahwa untuk gas hydrogen, nilai Z lebih besar daripada zat lain pada semua rentang tekanan. Untuk gas nitrogen, nilai Z lebih kecil dari pada satu pada tekanan rendah, tetapi lebih besar daripada satu pada tekanan tinggi. Gas metana dan karbondioksida
14 │Dr. Sanjaya, M.Si., M. Hadeli. L.,M.Si.Ph.D, dkk