Page 39 - Ebook Kesetimbangan Kimia
P. 39
Untuk menggambarkan hal ini, telah dilakukan tiga percobaan
yang berbeda seperti yang dapat dilihat pada Tabel 1. 1
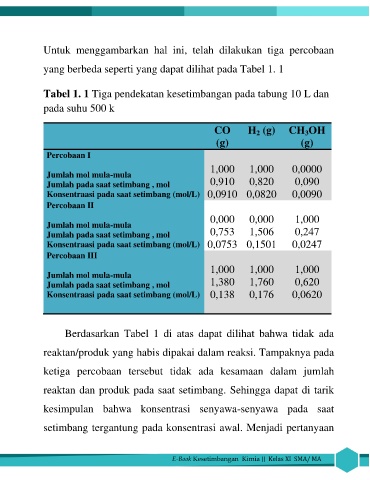
Tabel 1. 1 Tiga pendekatan kesetimbangan pada tabung 10 L dan
pada suhu 500 k
CO H (g) CH OH
2
3
(g) (g)
Percobaan I
1,000 1,000 0,0000
Jumlah mol mula-mula
Jumlah pada saat setimbang , mol 0,910 0,820 0,090
Konsentraasi pada saat setimbang (mol/L) 0,0910 0,0820 0,0090
Percobaan II
0,000 0,000 1,000
Jumlah mol mula-mula
Jumlah pada saat setimbang , mol 0,753 1,506 0,247
Konsentraasi pada saat setimbang (mol/L) 0,0753 0,1501 0,0247
Percobaan III
1,000 1,000 1,000
Jumlah mol mula-mula
Jumlah pada saat setimbang , mol 1,380 1,760 0,620
Konsentraasi pada saat setimbang (mol/L) 0,138 0,176 0,0620
Berdasarkan Tabel 1 di atas dapat dilihat bahwa tidak ada
reaktan/produk yang habis dipakai dalam reaksi. Tampaknya pada
ketiga percobaan tersebut tidak ada kesamaan dalam jumlah
reaktan dan produk pada saat setimbang. Sehingga dapat di tarik
kesimpulan bahwa konsentrasi senyawa-senyawa pada saat
setimbang tergantung pada konsentrasi awal. Menjadi pertanyaan
E-Book Kesetimbangan Kimia ∣∣ Kelas XI SMA/ MA