Page 93 - 《化學觀念總整理 1 》
P. 93
十四、化學式
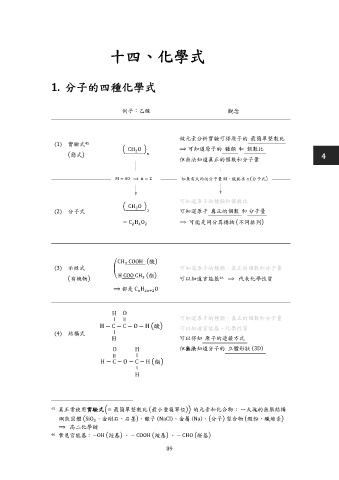
1. 分子的四種化學式
例子:乙酸 觀念
做元素分析實驗可得原子的 最簡單整數比
(1) 實驗式
45
CH O ⟹ 可知道原子的 種類 和 個數比
簡式 4
但無法知道真正的個數和分子量
M ≈ 60 ⟹ n = 2 如果有大約的分子量 M,就能求 n 分子式
可知道原子的種類和個數比
CH O
(2) 分子式 可知道原子 真正的個數 和 分子量
= C H O ⟹ 可能是同分異構物 不同排列
CH COOH 酸
(3) 示性式 可知道原子的種類、真正的個數和分子量
H COO CH 酯
46
有機物 可以知道官能基 ⟹ 代表化學性質
⟹ 都是 C H O
− − H = 可知道原子的種類、真正的個數和分子量
O
H − C − C − O − H 酸 可以知道官能基、化學性質
(4) 結構式
H 可以得知 原子的連接方式
O 但無法知道分子的 立體形狀 (3D)
− − H
=
H − C − O − C − H 酯
H
45 真正常使用實驗式 = 最簡單整數比 最小重複單位 的元素和化合物 ∶ 一大塊的無限結構
網狀固體 SiO 、金剛石、石墨 、離子 (NaCl)、金屬 (Na)、 分子 聚合物 澱粉、纖維素
⟹ 高二化學鍵
46 常見官能基 ∶ −OH 羥基 、 − COOH 羧基 、 − CHO 醛基
89