Page 22 - BUKU ELEKTRONIK KESETIMBANGAN KIMIA KELAS XI
P. 22
Buku Kimia SMA XI Berkonteks Lingkungan
Reaksi ini berakhir dengan suatu kesetimbangan atau menuju keadaan setimbang, yaitu
jika tidak terjadi lagi perubahan makroskopis, yang dapat dilihat dari warna zat tidak menjadi
cokelat tua atau cokelat muda, konsentrasinya pun menjadi tetap. Pada keadaan setimbang tidak
terjadi perubahan konsentrasi walaupun secara mikroskopis reaksi tetap berlangsung.
Perhatikan grafik perubahan konsentrasi gas N2O4 dan gas NO2 terhadap waktu dan grafik
laju reaksi terhadap waktu pada Gambar 2.3!
Berdasarkan contoh reaksi kesetimbangan tersebut, dapat disimpulkan bahwa pada reaksi
kesetimbangan terjadi sebagai berikut.
a. Pada suatu saat, jumlah larutan atau konsentrasi larutan tidak berubah lagi, perbandingan
konsentrasi konstan
b. Reaksi berlangsung dalam dua arah, ke kanan dan ke kiri, yang berlangsung terus-
menerus, sampai pada kondisi laju reaksi ke kanan sama dengan laju reaksi ke kiri walau
jumlah dan hasil reaksi tidak sama.
c. Baik reaktan maupun produk tidak keluar dari sistem.
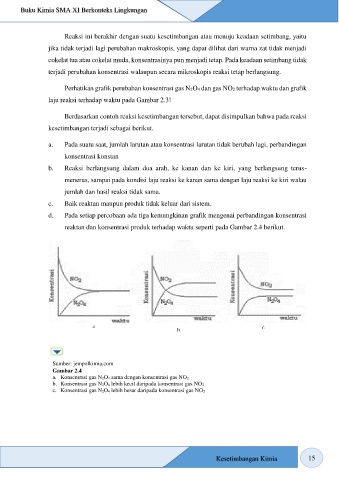
d. Pada setiap percobaan ada tiga kemungkinan grafik mengenai perbandingan konsentrasi
reaktan dan konsentrasi produk terhadap waktu seperti pada Gambar 2.4 berikut.
a b c
Sumber: jempolkimia.com
Gambar 2.4
a. Konsentrasi gas N2O4 sama dengan konsentrasi gas NO2
b. Konsentrasi gas N2O4 lebih kecil daripada konsentrasi gas NO 2
c. Konsentrasi gas N2O4 lebih besar daripada konsentrasi gas NO 2
Kesetimbangan Kimia 15