Page 33 - E-Modul Reaksi Redoks Kelas X
P. 33
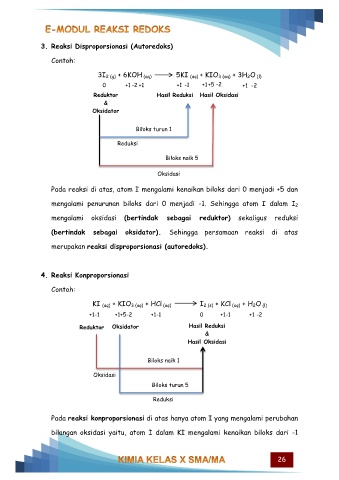
3. Reaksi Disproporsionasi (Autoredoks)
Contoh:
3I 2 (g) + 6KOH (aq) 5KI (aq) + KIO 3 (aq) + 3H 2O (l)
0 +1 -2 +1 +1 -1 +1 +5 -2 +1 -2
Reduktor Hasil Reduksi Hasil Oksidasi
&
Oksidator
Biloks turun 1
Reduksi
Biloks naik 5
Oksidasi
Pada reaksi di atas, atom I mengalami kenaikan biloks dari 0 menjadi +5 dan
mengalami penurunan biloks dari 0 menjadi -1. Sehingga atom I dalam I 2
mengalami oksidasi (bertindak sebagai reduktor) sekaligus reduksi
(bertindak sebagai oksidator). Sehingga persamaan reaksi di atas
merupakan reaksi disproporsionasi (autoredoks).
4. Reaksi Konproporsionasi
Contoh:
KI (aq) + KIO 3 (aq) + HCl (aq) I 2 (s) + KCl (aq) + H 2O (l)
+1-1 +1+5-2 +1-1 0 +1-1 +1 -2
Reduktor Oksidator Hasil Reduksi
&
Hasil Oksidasi
Biloks naik 1
Oksidasi
Biloks turun 5
Reduksi
Pada reaksi konproporsionasi di atas hanya atom I yang mengalami perubahan
bilangan oksidasi yaitu, atom I dalam KI mengalami kenaikan biloks dari -1
26