Page 17 - E-Book Sistem Pernapasan untuk Melatih Keterampilan Berpikir Kreatif SMA Kelas XI
P. 17
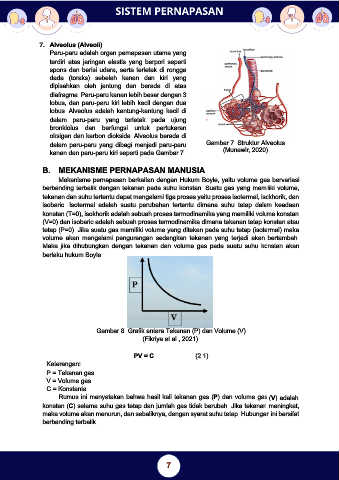
7. Alveolus (Alveoli)
Paru-paru adalah organ pernapasan utama yang
terdiri atas jaringan elastis yang berpori seperti
spons dan berisi udara, serta terletak di rongga
dada (toraks) sebelah kanan dan kiri yang
dipisahkan oleh jantung dan berada di atas
diafragma. Paru-paru kanan lebih besar dengan 3
lobus, dan paru-paru kiri lebih kecil dengan dua
lobus. Alveolus adalah kantung-kantung kecil di
dalam paru-paru yang terletak pada ujung
bronkiolus dan berfungsi untuk pertukaran
oksigen dan karbon dioksida. Alveolus berada di
dalam paru-paru yang dibagi menjadi paru-paru Gambar 7. Struktur Alveolus
kanan dan paru-paru kiri seperti pada Gambar 7. (Munawir, 2020)
B. MEKANISME PERNAPASAN MANUSIA
Mekanisme pernapasan berkaitan dengan Hukum Boyle, yaitu volume gas bervariasi
berbanding terbalik dengan tekanan pada suhu konstan. Suatu gas yang memiliki volume,
tekanan dan suhu tertentu dapat mengalami tiga proses yaitu proses isotermal, isokhorik, dan
isobaric. Isotermal adalah suatu perubahan tertentu dimana suhu tetap dalam keadaan
konstan (T=0), isokhorik adalah sebuah proses termodinamika yang memiliki volume konstan
(V=0) dan isobaric adalah sebuah proses termodinamika dimana tekanan tetap konstan atau
tetap (P=0). Jika suatu gas memiliki volume yang ditekan pada suhu tetap (isotermal) maka
volume akan mengalami pengurangan sedangkan tekanan yang terjadi akan bertambah.
Maka jika dihubungkan dengan tekanan dan volume gas pada suatu suhu konstan akan
berlaku hukum Boyle.
Gambar 8. Grafik antara Tekanan (P) dan Volume (V)
(Fikriya et al., 2021).
PV = C (2.1)
Keterangan:
P = Tekanan gas
V = Volume gas
C = Konstanta
Rumus ini menyatakan bahwa hasil kali tekanan gas (P) dan volume gas (V) adalah
konstan (C) selama suhu gas tetap dan jumlah gas tidak berubah. Jika tekanan meningkat,
maka volume akan menurun, dan sebaliknya, dengan syarat suhu tetap. Hubungan ini bersifat
berbanding terbalik.
7