Page 3 - BAHAN AJAR
P. 3
MODUL
dalam pelarut. Sementara partikel-partikel pelarut di fase gas yang dekat dengan
permukaan fase cair dapat terperangkap oleh ikatan antarA partikel dalam pelarut dan pergi
ke fase cair. Energi yang diperlukan untuk melepaskan ikatan antar partikel dalam pelarut
dapat berasal dari pemanasan. Pemanasan dapat berakibat semakin banyak partikel yang
pergi kefase gas. Oleh karena itu, tekanan uap pada suhu tinggi akan semakin besar
Pada alat tersebut setelah larutan dimasukkan dalam labu, semua udara dalam pipa
penghubung dikeluarkan melalui pompa vakum. Jika keran ditutup, maka uap yang ada
dalam pipa penghubung hanyalah uap dari pelarut larutan tadi sehingga uap itu disebut
tekanan uap larutan tersebut. Semakin tinggi suhu cairan semakin banyak uap yang berada
di atas permukaan cairan dan tekanan uap yang terbaca semakin tinggi.
Tabel 1. Tekanan Uap Air pada Berbagai Suhu (mmHg)
T (°C) P T (°C) P T (°C) P T (°C) P
0 4,58 21 18,65 35 42,2 92 567,0
5 6,54 22 19,83 40 55,3 94 610,9
10 9,21 23 21,07 45 71,9 96 657,6
12 10,52 24 22,38 50 97,5 98 707,3
14 11,99 25 23,76 55 118,0 100 760,0
16 13,63 26 25,21 60 149,4 102 815,9
17 14,53 27 26,74 65 187,5 104 875,1
18 15,48 28 28,35 70 233,7 106 973,9
19 16,84 29 30,04 80 355,1 108 1004,6
20 17,54 30 31,82 90 525,8 110 1074,6
TEKANAN UAP LARUTAN
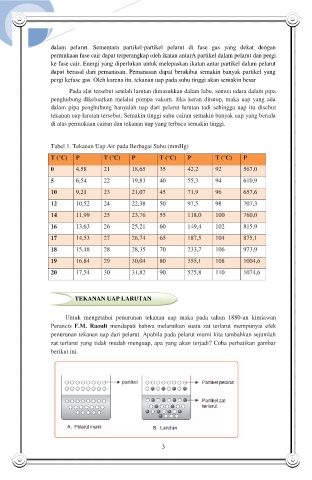
Untuk mengetahui penurunan tekanan uap maka pada tahun 1880-an kimiawan
Perancis F.M. Raoult mendapati bahwa melarutkan suatu zat terlarut mempunyai efek
penurunan tekanan uap dari pelarut. Apabila pada pelarut murni kita tambahkan sejumlah
zat terlarut yang tidak mudah menguap, apa yang akan terjadi? Coba perhatikan gambar
berikut ini.
3