Page 5 - BAHAN AJAR
P. 5
MODUL
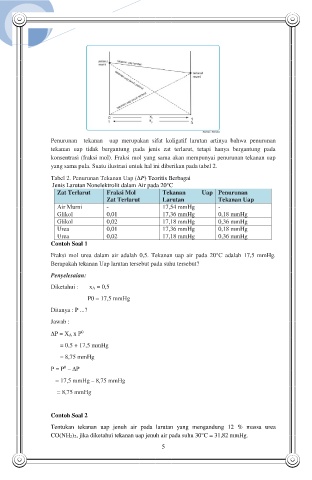
Penurunan tekanan uap merupakan sifat koligatif larutan artinya bahwa penurunan
tekanan uap tidak bergantung pada jenis zat terlarut, tetapi hanya bergantung pada
konsentrasi (fraksi mol). Fraksi mol yang sama akan mempunyai penurunan tekanan uap
yang sama pula. Suatu ilustrasi untuk hal ini diberikan pada tabel 2.
Tabel 2. Penurunan Tekanan Uap (P) Teoritis Berbagai
Jenis Larutan Nonelektrolit dalam Air pada 20°C
Zat Terlarut Fraksi Mol Tekanan Uap Penurunan
Zat Terlarut Larutan Tekanan Uap
Air Murni - 17,54 mmHg -
Glikol 0,01 17,36 mmHg 0,18 mmHg
Glikol 0,02 17,18 mmHg 0,36 mmHg
Urea 0,01 17,36 mmHg 0,18 mmHg
Urea 0,02 17,18 mmHg 0,36 mmHg
Contoh Soal 1
Fraksi mol urea dalam air adalah 0,5. Tekanan uap air pada 20°C adalah 17,5 mmHg.
Berapakah tekanan Uap larutan tersebut pada suhu tersebut?
Penyelesaian:
Diketahui : xA = 0,5
P0 = 17,5 mmHg
Ditanya : P ...?
Jawab :
0
P = XA x P
= 0,5 + 17,5 mmHg
= 8,75 mmHg
0
P = P – P
= 17,5 mmHg – 8,75 mmHg
= 8,75 mmHg
Contoh Soal 2
Tentukan tekanan uap jenuh air pada larutan yang mengandung 12 % massa urea
CO(NH2)2, jika diketahui tekanan uap jenuh air pada suhu 30°C = 31,82 mmHg.
5