Page 30 - E-MODUL ASAM BASA SENYAWA ORGANIK_ANDRA MEISANTRY ASSARI_F1062181002_P. KIMIA
P. 30
Karena klorin lebih elektronegatif dibandingkan karbon, ikatan C─Cl
terpolarisasi dengan klorin membawa muatan negatif parsial dan karbon positif
parsial. Jadi, elektron tertarik menjauhi ujung ion karboksilat kearah klorin. Efek
ini cenderung menyebarkan muatan negatif pada atom yang lebih banyak
dibandingkan pada ion asetat sendiri dan dengan demikian menstabilkan ion yang
bersangkutan. Semakin banyak klorin, semakin besar efek dan semakin besar
kekuatan asam.
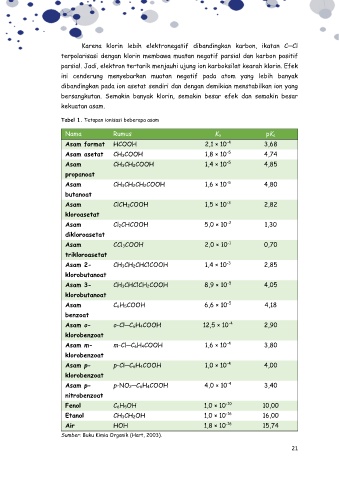
Tabel 1. Tetapan ionisasi beberapa asam
Nama Rumus Ka pKa
Asam format HCOOH 2,1 × 10 -4 3,68
-5
Asam asetat CH3COOH 1,8 × 10 4,74
-5
Asam CH3CH2COOH 1,4 × 10 4,85
propanoat
-5
Asam CH3CH2CH2COOH 1,6 × 10 4,80
butanoat
Asam ClCH2COOH 1,5 × 10 2,82
-3
kloroasetat
-2
Asam Cl2CHCOOH 5,0 × 10 1,30
dikloroasetat
-1
Asam CCl3COOH 2,0 × 10 0,70
trikloroasetat
-3
Asam 2- CH3CH2CHClCOOH 1,4 × 10 2,85
klorobutanoat
Asam 3- CH3CHClCH2COOH 8,9 × 10 4,05
-5
klorobutanoat
Asam C6H5COOH 6,6 × 10 4,18
-5
benzoat
-4
Asam o- o-Cl─C6H4COOH 12,5 × 10 2,90
klorobenzoat
-4
Asam m- m-Cl─C6H4COOH 1,6 × 10 3,80
klorobenzoat
Asam p- p-Cl─C6H4COOH 1,0 × 10 4,00
-4
klorobenzoat
-4
Asam p- p-NO2─C6H4COOH 4,0 × 10 3,40
nitrobenzoat
-10
Fenol C6H5OH 1,0 × 10 10,00
-16
Etanol CH3CH2OH 1,0 × 10 16,00
Air HOH 1,8 × 10 15,74
-16
Sumber: Buku Kimia Organik (Hart, 2003).
21