Page 10 - Herlihy: The Human Body in Health and Illness, 3rd Edition
P. 10
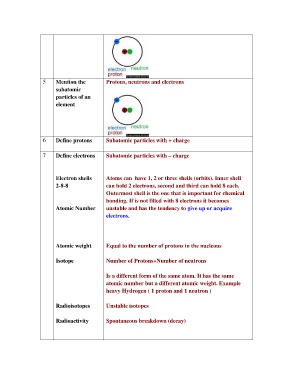
5 Mention the Protons, neutrons and electrons
subatomic
particles of an
element
6 Define protons Subatomic particles with + charge
7 Define electrons Subatomic particles with – charge
Electron shells Atoms can have 1, 2 or three shells (orbits). Inner shell
288 can hold 2 electrons, second and third can hold 8 each.
Outermost shell is the one that is important for chemical
bonding. If is not filled with 8 electrons it becomes
Atomic Number unstable and has the tendency to give up or acquire
electrons.
Atomic weight Equal to the number of protons in the nucleous
Isotope Number of Protons+Number of neutrons
Is a different form of the same atom. It has the same
atomic number but a different atomic weight. Example
heavy Hydrogen ( 1 proton and 1 neutron )
Radioisotopes Unstable isotopes
Radioactivity Spontaneous breakdown (decay)