Page 5 - Demo
P. 5
107
106
105
104
103
102
101
100
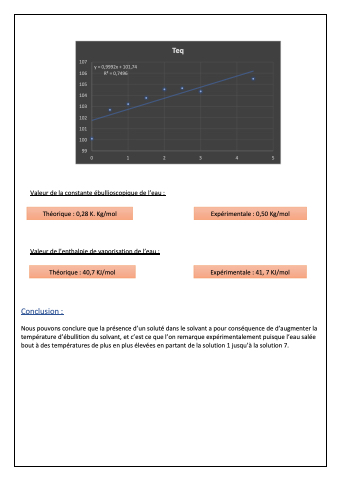
Teq
y = 0,9992x + 101,74 R2 = 0,7496
99
012345
Valeur de la constante ébullioscopique de l’eau :
Théorique : 0,28 K. Kg/mol
Valeur de l’enthalpie de vaporisation de l’eau :
Conclusion :
Nous pouvons conclure que la présence d’un soluté dans le solvant a pour conséquence de d’augmenter la température d’ébullition du solvant, et c’est ce que l’on remarque expérimentalement puisque l’eau salée bout à des températures de plus en plus élevées en partant de la solution 1 jusqu’à la solution 7.
Expérimentale : 0,50 Kg/mol
Théorique : 40,7 KJ/mol
Expérimentale : 41, 7 KJ/mol