Page 18 - E-Modul Laju Reaksi html
P. 18
3. Konsentrasi
Reaksi kimia akan berlangsung lebih cepat apabila
konsentrasi dari zat yang bereaksi lebih besar. Hal ini
dikarenakan semakin besar konsentrasi, maka akan semakin
banyak jumlah partikel zat sehingga semakin banyak pula
tumbukan efektif yang terjadi. Dengan demikian reaksi akan
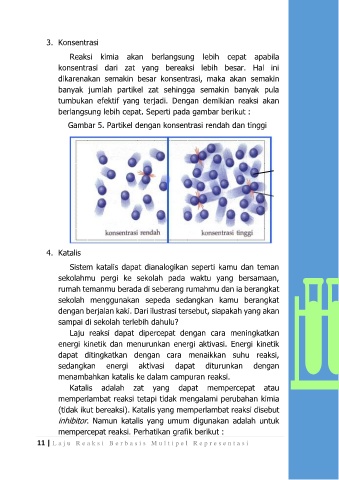
berlangsung lebih cepat. Seperti pada gambar berikut :
Gambar 5. Partikel dengan konsentrasi rendah dan tinggi
4. Katalis
Sistem katalis dapat dianalogikan seperti kamu dan teman
sekolahmu pergi ke sekolah pada waktu yang bersamaan,
rumah temanmu berada di seberang rumahmu dan ia berangkat
sekolah menggunakan sepeda sedangkan kamu berangkat
dengan berjalan kaki. Dari ilustrasi tersebut, siapakah yang akan
sampai di sekolah terlebih dahulu?
Laju reaksi dapat dipercepat dengan cara meningkatkan
energi kinetik dan menurunkan energi aktivasi. Energi kinetik
dapat ditingkatkan dengan cara menaikkan suhu reaksi,
sedangkan energi aktivasi dapat diturunkan dengan
menambahkan katalis ke dalam campuran reaksi.
Katalis adalah zat yang dapat mempercepat atau
memperlambat reaksi tetapi tidak mengalami perubahan kimia
(tidak ikut bereaksi). Katalis yang memperlambat reaksi disebut
.
inhibitor Namun katalis yang umum digunakan adalah untuk
mempercepat reaksi. Perhatikan grafik berikut :
11 | L a j u R e a k s i B e r b a s i s M u l t i p e l R e p r e s e n t a s i