Page 15 - E-Modul Kesetimbangan Kimia
P. 15
B. Kesetimbangan Dinamis
Kesetimbangan kimia bersifat dinamis artinya reaksi tetap berjalan pada tingkat
mikroskopis (molekul).
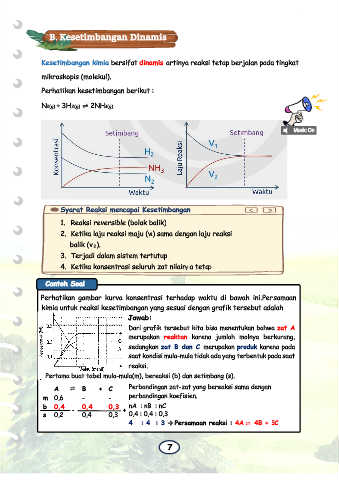
Perhatikan kesetimbangan berikut :
N2(g) + 3H2(g) ⇌ 2NH3(g).
Syarat Reaksi mencapai Kesetimbangan
1. Reaksi reversible (bolak balik)
2. Ketika laju reaksi maju (v1) sama dengan laju reaksi
balik (v2).
3. Terjadi dalam sistem tertutup
4. Ketika konsentrasi seluruh zat nilainya tetap
Contoh Soal
Perhatikan gambar kurva konsentrasi terhadap waktu di bawah ini.Persamaan
kimia untuk reaksi kesetimbangan yang sesuai dengan grafik tersebut adalah
Jawab:
Dari grafik tersebut kita bisa menentukan bahwa zat A
merupakan reaktan karena jumlah molnya berkurang,
sedangkan zat B dan C merupakan produk karena pada
saat kondisi mula-mula tidak ada yang terbentuk pada saat
reaksi.
Pertama buat tabel mula-mula(m), bereaksi (b) dan setimbang (s).
A ⇌ B + C Perbandingan zat-zat yang bereaksi sama dengan
m 0,6
- - perbandingan koefisien.
b 0,4 0,4 0,3 nA : nB : nC
s 0,2 - 0,4 0,3 + 0,4 : 0,4 : 0,3
4 : 4 : 3 → Persamaan reaksi : 4A ⇌ 4B + 3C
7