Page 49 - E-BOOK INTERAKTIF BERORIENTASI EVERYDAY LIFE PHENOMENA PADA MATERI ASAM BASA
P. 49
Reaksi ionisasi air merupakan reaksi endoterm sehingga bila suhunya naik, nilai Kw akan
0
semakin besar, pada suhu 25 C, nilai Kw adalah 10 -14 . Konstanta kesetimbangan Kw
+
juga dinamakan konstanta hasilkali ion, yaitu hasilkali antara konsentrasi ion H dan
-
+
-
ion OH pada suhu tertentu. Apabila [H ] = [OH ] maka larutan dalam pelarut air
dikatakan netral.
Setelah mendapatkan nilai Kw, mari kita kembali sejenak pada materi konsep pH
larutan. Sebelumnya Anda sudah mengetahui hubungan antara pH larutan dengan
konsentrasi ion H , lalu bagaimana hubungan pH dengan konsentrasi ion OH . Apakah
+
-
+
hubungan keduanya sama seperti hubungan antara pH dan konsetrasi ion H ?
-
Untuk mengetahuinya, tentukanlah terlebih dahulu konsentrasi ion OH pada larutan
NaOH untuk masing-masing konsentrasi!
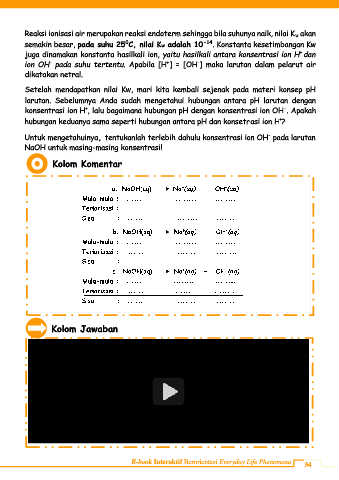
Kolom Komentar
+
a. NaOH(aq) Na (aq) + OH (aq)
-
Mula-mula : .......... ............. .............
Terionisasi : .......... ............ .............
Sisa : .......... ............. .............
+
-
b. NaOH(aq) Na (aq) + OH (aq)
Mula-mula : .......... ............. .............
Terionisasi : .......... ............ .............
Sisa : .......... ............. .............
+
c. NaOH(aq) Na (aq) + OH (aq)
-
Mula-mula : .......... ............. .............
Terionisasi : .......... ............ .............
Sisa : .......... ............. .............
Kolom Jawaban
-
+
a. NaOH(aq) Na (aq) + OH (aq)
Mula-mula : 0,1M 0 0
Terionisasi : 0,1M 0,1M 0,1M
Sisa : 0 0,1M 0,1M
b. NaOH(aq) Na (aq) + OH (aq)
-
+
Mula-mula : 0,01M 0 0
Terionisasi : 0,01M 0,01M 0,01M
Sisa : 0 0,01M 0,01M
+
-
c. NaOH(aq) Na (aq) + OH (aq)
Mula-mula : 0,001M 0 0
Terionisasi : 0,001M 0,001M 0,001M
Sisa : 0 0,001M 0,001M
E-book Interaktif Berorientasi Everyday Life Phenomena 34