Page 13 - Modul Asam Basa Februari
P. 13
Dari Peristiwa ini munculah sebuah teori baru yang
dikemukakan oleh Johanes N. Bronsted dan Thomas M. Lowry
dari inggris pada tahun 1923. Mereka menyatakan bahwa sifat
asam dan basa ditentukan oleh kemampuan senyawa mlepas
atau menerima proton (H+) :
”Asam merupakan senyawa atau partikel yang dapat
memberikan proton, H+ (donor proton) kepada senyawa atau
partikel lain. Basa adalah senyawa atau partikel yang dapat
menerima proton, H+ (akseptor proton) dari asam”
Teori tersebut dapat menggambarkan reaksi amonia sebagai
basa dengan cara sebagai berikut :
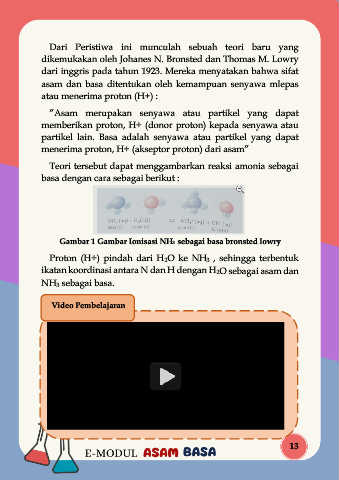
Gambar 1 Gambar Ionisasi NH3 sebagai basa bronsted lowry
Proton (H+) pindah dari H2O ke NH3 , sehingga terbentuk
ikatan koordinasi antara N dan H dengan H2O sebagai asam dan
NH3 sebagai basa.
Video Pembelajaran
13