Page 45 - E-MODUL ASAM BASA SENYAWA ORGANIK_ANDRA MEISANTRY ASSARI_F1062181002_PENDIDIKAN KIMIA
P. 45
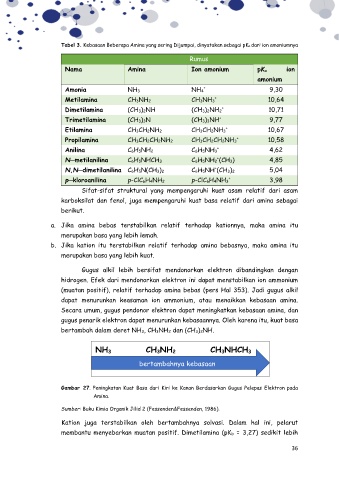
Tabel 3. Kebasaan Beberapa Amina yang sering Dijumpai, dinyatakan sebagai pKa dari ion amoniumnya
Rumus
Nama Amina Ion amonium pKa ion
amonium
+
Amonia NH3 NH4 9,30
Metilamina CH3NH2 CH3NH3 + 10,64
Dimetilamina (CH3)2NH (CH3)2NH2 + 10,71
Trimetilamina (CH3)3N (CH3)3NH + 9,77
Etilamina CH3CH2NH2 CH3CH2NH3 + 10,67
Propilamina CH3CH2CH2NH2 CH3CH2CH2NH3 + 10,58
Anilina C6H5NH2 C6H5NH3 + 4,62
N─metilanilina C6H5NHCH3 C6H5NH2 (CH3) 4,85
+
N,N─dimetilanilina C6H5N(CH3)2 C6H5NH (CH3)2 5,04
+
p─kloroanilina p-ClC6H4NH2 p-ClC6H4NH3 + 3,98
Sifat-sifat struktural yang mempengaruhi kuat asam relatif dari asam
karboksilat dan fenol, juga mempengaruhi kuat basa relatif dari amina sebagai
berikut.
a. Jika amina bebas terstabilkan relatif terhadap kationnya, maka amina itu
merupakan basa yang lebih lemah.
b. Jika kation itu terstabilkan relatif terhadap amina bebasnya, maka amina itu
merupakan basa yang lebih kuat.
Gugus alkil lebih bersifat mendonorkan elektron dibandingkan dengan
hidrogen. Efek dari mendonorkan elektron ini dapat menstabilkan ion ammonium
(muatan positif), relatif terhadap amina bebas (pers Hal 353). Jadi gugus alkil
dapat menurunkan keasaman ion ammonium, atau menaikkan kebasaan amina.
Secara umum, gugus pendonor elektron dapat meningkatkan kebasaan amina, dan
gugus penarik elektron dapat menurunkan kebasaannya. Oleh karena itu, kuat basa
bertambah dalam deret NH3, CH3NH2 dan (CH3)2NH.
NH 3 CH 3NH 2 CH 3NHCH 3
bertambahnya kebasaan
Gambar 27. Peningkatan Kuat Basa dari Kiri ke Kanan Berdasarkan Gugus Pelepas Elektron pada
Amina.
Sumber: Buku Kimia Organik Jilid 2 (Fessenden&Fessenden, 1986).
Kation juga terstabilkan oleh bertambahnya solvasi. Dalam hal ini, pelarut
membantu menyebarkan muatan positif. Dimetilamina (pKb = 3,27) sedikit lebih
36