Page 59 - BUKU ELEKTRONIK KIMIA BERBASIS KONTEKSTUAL KELAS X SMA/MA
P. 59
Garam di dalam air akan mengalami ionisasi menjadi ion logam dan ion sisa asam.
Contoh:
KNO3 (aq) → K+ (aq) + NO3¯ (aq)
2+
Ca(ClO)2(aq) → Ca (aq) + 2 ClO¯(aq)
3+
2-
Al2(SO4)3(aq) → 2 Al (aq) + 3 SO4 (aq)
Secara umum pembentukan garam atau senyawa elektrolit dapat dituliskan sebagai
berikut:
Jelajah Kimia
x+
y-
y A + x B → AyBx
Keterangan:
x+
A = kation Temukan informasi lebih
lanjut mengenai bilangan
B y- = anion
oksidasi di:
x+ = jumlah muatan kation
http://www.chemguide.co.uk/
y- = jumlah muatan anion inorganic/redox/oxidnstates.
AyBx = rumus senyawa (jumlah muatan (+) dan (-) adalah html
nol (0))
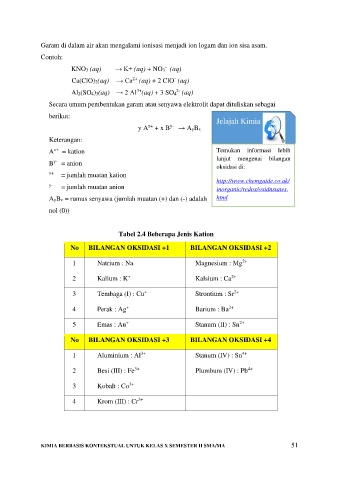
Tabel 2.4 Beberapa Jenis Kation
No BILANGAN OKSIDASI +1 BILANGAN OKSIDASI +2
2+
1 Natrium : Na Magnesium : Mg
+
2+
2 Kalium : K Kalsium : Ca
2+
+
3 Tembaga (I) : Cu Strontium : Sr
+
2+
4 Perak : Ag Barium : Ba
+
2+
5 Emas : Au Stanum (II) : Sn
No BILANGAN OKSIDASI +3 BILANGAN OKSIDASI +4
3+
4+
1 Aluminium : Al Stanum (IV) : Sn
4+
2 Besi (III) : Fe 3+ Plumbum (IV) : Pb
3+
3 Kobalt : Co
3+
4 Krom (III) : Cr
KIMIA BERBASIS KONTEKSTUAL UNTUK KELAS X SEMESTER II SMA/MA 51