Page 14 - E-MODUL STEM-PJBL UNSUR GOLONGAN HALOGEN
P. 14
"lahir" atau "terbentuk". Dengan kata lain, halogen berarti "pembentuk garam", yang
setidaknya sebagian menggambarkan perilaku kimianya. Anggota golongan Halogen
terdiri fluor (F), klor (Cl), brom (Br), iod (I), dan astatin (At). Fluorin dan Klorin
merupakan gas yang bersifat volatile, iodin merupakan padatan yang mudah menyublim,
sedangkan astatin merupakan unsur radioaktif dengan waktu hidup (life time) yang sangat
singkat sehingga segera meluruh menjadi unsur lain. Semua unsur halogen bersifat
nonlogam, kecuali At yang bersifat semilogam atau (metalloid). Semua unsurnya
bereaksi langsung dengan logam membentuk garam. Kereaktifan yang sangat tinggi
mengakibatkan halogen tidak dijumpai sebagai atom bebas di alam, melainkan dalam
bentuk senyawa-senyawa garamnya, yaitu garam halida. Fluorin dikenal sebagai unsur
paling reaktif.
Unsur-Unsur Halogen memiliki sifat yang sangat mirip satu sama lain. Sesuai
dengan nomor golongannya, semua unsur halogen memiliki tujuh elektron valensi, dua
elektron dalam orbital s dan lima elektron dalam orbital p. Konfigurasi elektron halogen
2
5
adalah ns np , Untuk membentuk struktur gas mulia, halogen kekurangan satu elektron
sehingga untuk mencapai oktet unsur halogen menarik satu elektron dari luar
-
menyebabkan terbentuk ion negatif (X ) untuk ikatan ionik atau dengan pemakaian
bersama pasangan elektron dengan atom lain untuk pembentukan ikatan kovalen.
Senyawa-senyawa dengan logam mempunyai sifat ionik sementara dengan nonlogam
memiliki sifat kovalen. Semua halogen membentuk senyawa stabil pada keadaan oksidasi
-1. Senyawa fluorin, hanya memiliki satu keadaan oksidasi yaitu -1, sedangkan klorin,
bromin dan iodin selain memiliki keadaan oksidasi -1, juga memiliki sederetan keadaan
oksidasi lain, yaitu +1, +3, +5, atau +7.
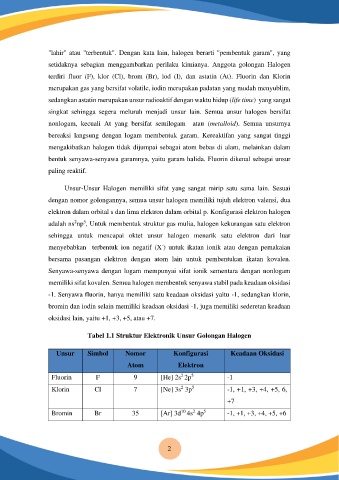
Tabel 1.1 Struktur Elektronik Unsur Golongan Halogen
Unsur Simbol Nomor Konfigurasi Keadaan Oksidasi
Atom Elektron
2
Fluorin F 9 [He] 2s 2p 5 -1
2
5
Klorin Cl 7 [Ne] 3s 3p -1, +1, +3, +4, +5, 6,
+7
2
5
10
Bromin Br 35 [Ar] 3d 4s 4p -1, +1, +3, +4, +5, +6
2