Page 65 - Kimia 1
P. 65
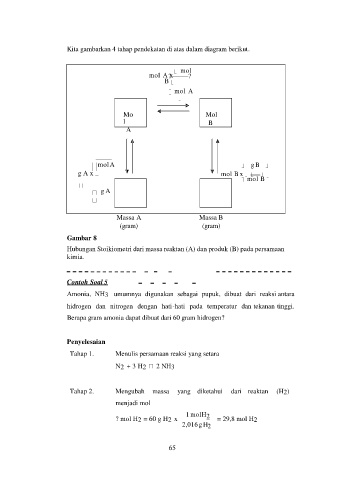
Kita gambarkan 4 tahap pendekatan di atas dalam diagram berikut.
mol
mol A x
B
mol A
Mo Mol
l B
A
mol A g B
g A x mol B x
mol B
g A
Massa A Massa B
(gram) (gram)
Gambar 8
Hubungan Stoikiometri dari massa reaktan (A) dan produk (B) pada persamaan
kimia.
Contoh Soal 5
Amonia, NH3 umumnya digunakan sebagai pupuk, dibuat dari reaksi antara
hidrogen dan nitrogen dengan hati-hati pada temperatur dan tekanan tinggi.
Berapa gram amonia dapat dibuat dari 60 gram hidrogen?
Penyelesaian
Tahap 1. Menulis persamaan reaksi yang setara
N2 + 3 H2 2 NH3
Tahap 2. Mengubah massa yang diketahui dari reaktan (H2)
menjadi mol
1 mol H
? mol H2 = 60 g H2 x 2 = 29,8 mol H2
2,016 g H
2
65