Page 29 - Modul Struktur Atom
P. 29
1. Jika s + d = 9, golongan VIIIB
2. Jika s + d = 10, golongan VIIIB
3. Jika s + d = 11, golongan IB
4. Jika s + d = 12, golongan IIB
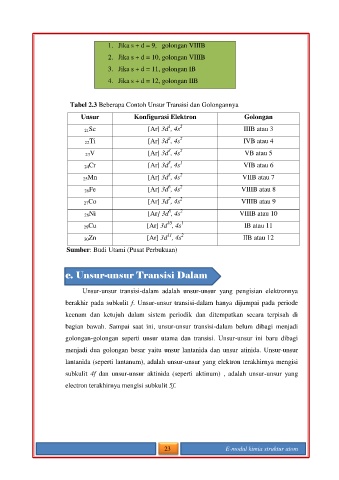
Tabel 2.3 Beberapa Contoh Unsur Transisi dan Golongannya
Unsur Konfigurasi Elektron Golongan
1
2
21Sc [Ar] 3d , 4s IIIB atau 3
2
2
22Ti [Ar] 3d , 4s IVB atau 4
3
2
23V [Ar] 3d , 4s VB atau 5
1
5
24Cr [Ar] 3d , 4s VIB atau 6
2
5
25Mn [Ar] 3d , 4s VIIB atau 7
6
2
26Fe [Ar] 3d , 4s VIIIB atau 8
2
7
27Co [Ar] 3d , 4s VIIIB atau 9
8
2
28Ni [Ar] 3d , 4s VIIIB atau 10
10
1
29Cu [Ar] 3d , 4s IB atau 11
2
11
30Zn [Ar] 3d , 4s IIB atau 12
Sumber: Budi Utami (Pusat Perbukuan)
c. Unsur-unsur Transisi Dalam
Unsur-unsur transisi-dalam adalah unsur-unsur yang pengisian elektronnya
berakhir pada subkulit f. Unsur-unsur transisi-dalam hanya dijumpai pada periode
keenam dan ketujuh dalam sistem periodik dan ditempatkan secara terpisah di
bagian bawah. Sampai saat ini, unsur-unsur transisi-dalam belum dibagi menjadi
golongan-golongan seperti unsur utama dan transisi. Unsur-unsur ini baru dibagi
menjadi dua golongan besar yaitu unsur lantanida dan unsur atinida. Unsur-unsur
lantanida (seperti lantanum), adalah unsur-unsur yang elektron terakhirnya mengisi
subkulit 4f dan unsur-unsur aktinida (seperti aktinum) , adalah unsur-unsur yang
electron terakhirnya mengisi subkulit 5f.
23 E-modul kimia struktur atom