Page 23 - E-MODUL LAJU REAKSI
P. 23
LANJUTAN
3. Orde reaksi dua
Orde reaksi dua menunjukkan bahwa laju reaksi merupakan pangkat dua dari konsentrasi
pereaksi.
D. Faktor-Faktor yang Memengaruhi Laju Reaksi
1. Konsentrasi : Jika konsentrasi pereaksi diperbesar, maka laju reaksi akan semakin cepat. Zat yang
lebih tinggi memiliki jumlah partikel yang lebih banyak dan rapat, sehingga tumbukan akan semakin
sering terjadi yang menyebabkan terjadinya reaksi kimia.
2. Luas permukaan sentuh zat: Semakin besar luas permukaan partikelnya, semakin tinggi frekuensi
tumbukan sehingga laju reaksi semakin cepat.
3. Suhu : Reaksi kimia akan berlangsung lebih cepat pada suhu yang tinggi. Laju reaksi bertambah cepat
jika suhu dinaikkan karena energy kenetik molekul akan meningkat. Energi kenetik yang meningkat
menyebabkan gerak partikel bertambah.
4. Katalis: Katalis adalah zat yang mampu mempercepat laju reaksi. Katalis ikut bereaksi, tetapi di akhir
reaksi, katalis terbentuk kembali seperti semula. Katalis dapat mempercepat laju reaksi dengan cara
membuat mekanisme reaksi alternatif dengan harga energi aktivasi yang lebih rendah. Dengan
rendahnya energi aktivasi maka tumbukan berlangsung lebih maksimal dan reaksi berlangsung lebih
cepat.
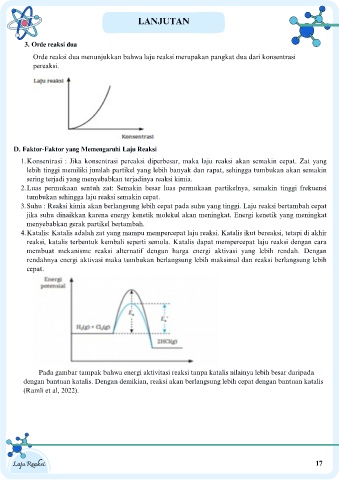
Pada gambar tampak bahwa energi aktivitasi reaksi tanpa katalis nilainya lebih besar daripada
dengan bantuan katalis. Dengan demikian, reaksi akan berlangsung lebih cepat dengan bantuan katalis
(Ramli et al, 2022).
Laju Reaksi 17