Page 21 - E MODUL AFIFAH KHAIRANI
P. 21
ASAM BASA
+ +
-
+
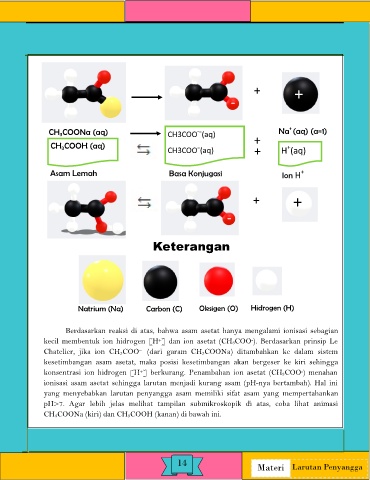
CH COONa (aq) CH3COO (aq) Na (aq) (a=1)
-=
3
CH COOH (aq) CH3COO (aq) + H (aq)
+
3
=
+
Asam Lemah Basa Konjugasi Ion H
+
+ +
-
Keterangan
Natrium (Na) Carbon (C) Oksigen (O) Hidrogen (H)
Berdasarkan reaksi di atas, bahwa asam asetat hanya mengalami ionisasi sebagian
kecil membentuk ion hidrogen [H ] dan ion asetat (CH3COO ). Berdasarkan prinsip Le
+
-
Chatelier, jika ion CH3COO (dari garam CH3COONa) ditambahkan ke dalam sistem
–
kesetimbangan asam asetat, maka posisi kesetimbangan akan bergeser ke kiri sehingga
konsentrasi ion hidrogen [H ] berkurang. Penambahan ion asetat (CH 3COO ) menahan
-
+
ionisasi asam asetat sehingga larutan menjadi kurang asam (pH-nya bertambah). Hal ini
yang menyebabkan larutan penyangga asam memiliki sifat asam yang mempertahankan
pH>7. Agar lebih jelas melihat tampilan submikroskopik di atas, coba lihat animasi
CH3COONa (kiri) dan CH3COOH (kanan) di bawah ini.
14 Materi Larutan Penyangga