Page 48 - cinetique FF_Neat
P. 48
1. Préciser le rôle de l’empois d’amidon et indiquer comment peut-on détecter
l’équivalence
2. Montrer que la concentration molaire en ions hypochlorite dans la solution d'eau de
Javel diluée est donnée par l'expression
ClO − = S 2 O 3 2− V (S 2 O 3 2− )
2V (eaudejavel )
Calculer numériquement cette concentration.
3. Est-il important d'introduire les ions iodure I en excès
-
II. Etude de la cinétique de décomposition de l’eau de Javel
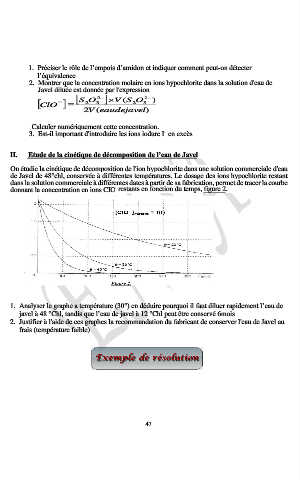
On étudie la cinétique de décomposition de l'ion hypochlorite dans une solution commerciale d'eau
de Javel de 48°chl, conservée à différentes températures. Le dosage des ions hypochlorite restant
dans la solution commerciale à différentes dates à partir de sa fabrication, permet de tracer la courbe
-
donnant la concentration en ions CIO restants en fonction du temps, figure 2.
1. Analyser le graphe a température (30°) en déduire pourquoi il faut diluer rapidement l’eau de
javel à 48 °Chl, tandis que l’eau de javel à 12 °Chl peut être conservé 6mois
2. Justifier à l'aide de ces graphes la recommandation du fabricant de conserver l'eau de Javel au
frais (température faible)
47