Page 13 - E-Modul Interaktif Reaksi Redoks
P. 13
b. Pengertian Reduksi
Sebaliknya, ketika sebuah atom, ion, atau molekul menjadi lebih
bermuatan negatif (menerima elektron), dapat dikatakan bahwa zat
tersebut telah tereduksi.
Reduksi adalah penerimaan elektron oleh atom suatu zat.
Ketika satu reaktan kehilangan elektron (yaitu, ketika dioksidasi),
reaktan lain harus menerima elektron tersebut (direduksi). Dengan kata lain
oksidasi dan reduksi selalu terjadi secara bersamaan.
c. Contoh-contoh Reaksi Redoks
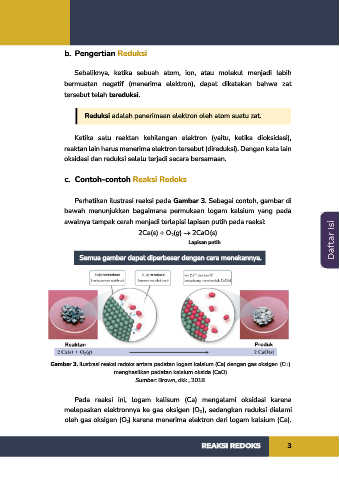
Perhatikan ilustrasi reaksi pada Gambar 3. Sebagai contoh, gambar di
bawah menunjukkan bagaimana permukaan logam kalsium yang pada
awalnya tampak cerah menjadi terlapisi lapisan putih pada reaksi:
2Ca(s) + O2(g) → 2CaO(s)
Lapisan putih
Semua gambar dapat diperbesar dengan cara menekannya.
Gambar 3. Ilustrasi reaksi redoks antara padatan logam kalsium (Ca) dengan gas oksigen (O 2)
menghasilkan padatan kalsium oksida (CaO)
Sumber: Brown, dkk., 2018
Pada reaksi ini, logam kalisum (Ca) mengalami oksidasi karena
melepaskan elektronnya ke gas oksigen (O2), sedangkan reduksi dialami
oleh gas oksigen (O2) karena menerima elektron dari logam kalsium (Ca).
REAKSI REDOKS 3