Page 116 - 00_sampul_depan.pdf
P. 116
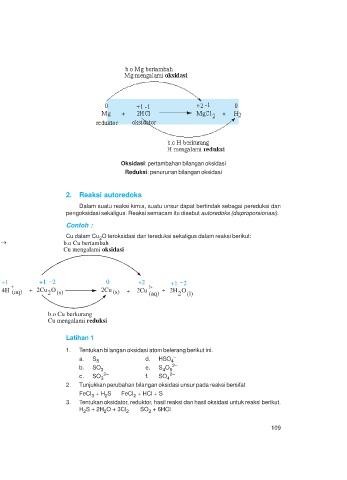
Oksidasi: pertambahan bilangan oksidasi
Reduksi: penurunan bilangan oksidasi
2. Reaksi autoredoks
Dalam suatu reaksi kimia, suatu unsur dapat bertindak sebagai pereduksi dan
pengoksidasi sekaligus. Reaksi semacam itu disebut autoredoks (disproporsionasi).
Contoh :
Cu dalam Cu O teroksidasi dan tereduksi sekaligus dalam reaksi berikut:
2
o o b.o Cu bertambah
Cu mengalami oksidasi
_
+1 +1 _ 2 0 +2 +1 2
4H + (aq) + 2Cu O 2Cu (s) + 2Cu 2+ + 2H O (l)
2 (s)
(aq)
2
b.o Cu berkurang
Cu mengalami reduksi
Latihan 1
1. Tentukan bilangan oksidasi atom belerang berikut ini.
a. S 8 d. HSO 4 –
b. SO 3 e. S O 2–
4 6
c. SO 3 2– f. SO 4 2–
2. Tunjukkan perubahan bilangan oksidasi unsur pada reaksi bersifat
FeCl + H S FeCl + HCl + S
2
3
2
3. Tentukan oksidator, reduktor, hasil reaksi dan hasil oksidasi untuk reaksi berikut.
H S + 2H O + 3Cl 2 SO + 6HCl
2
2
2
109