Page 23 - E-MODUL SIFAT ASAM BASA SENYAWA ORGANIK_ANDRA MEISANTRY ASSARI_F1062181002_FKIP
P. 23
Nilai pKa pada Tabel 1. merupakan nilai paling akurat karena dapat diukur di
dalam larutan berair. Berdasarkan data pada Tabel 1. dapat disimpulkan bahwa
semakin kecil pKa basa konjugatnya, maka semakin kuat asamnya. Begitu sebaliknya,
semakin besar pKa asam konjugatnya, maka semakin kuat basanya.
-
Faktor-faktor utama yang mempengaruhi kestabilan anion (A ), dan juga
mempengaruhi kuat asam HA, antara lain: 1) keelektronegatifan atom yang mengemban
muatan negatif dalam anion (A ); 2) ukuran anion (A ); 3) hibridisasi atom yang
-
-
-
mengemban muatan negatif dalam anion (A ); 4) efek induktif atom-atom atau gugus-
gugus lain yang terikat pada atom negatif dalam anion (A ); 5) stabilisasi-resonansi
-
-
anion (A ); dan 6) solvasi anion (A ). Faktor-faktor ini dapat mengacu pada Tabel
-
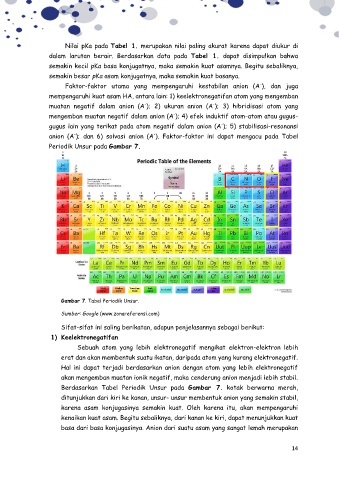
Periodik Unsur pada Gambar 7.
Gambar 7. Tabel Periodik Unsur.
Sumber: Google (www.zonareferensi.com)
Sifat-sifat ini saling berikatan, adapun penjelasannya sebagai berikut:
1) Keelektronegatifan
Sebuah atom yang lebih elektronegatif mengikat elektron-elektron lebih
erat dan akan membentuk suatu ikatan, daripada atom yang kurang elektronegatif.
Hal ini dapat terjadi berdasarkan anion dengan atom yang lebih elektronegatif
akan mengemban muatan ionik negatif, maka cenderung anion menjadi lebih stabil.
Berdasarkan Tabel Periodik Unsur pada Gambar 7. kotak berwarna merah,
ditunjukkan dari kiri ke kanan, unsur- unsur membentuk anion yang semakin stabil,
karena asam konjugasinya semakin kuat. Oleh karena itu, akan mempengaruhi
kenaikan kuat asam. Begitu sebaliknya, dari kanan ke kiri, dapat menunjukkan kuat
basa dari basa konjugasinya. Anion dari suatu asam yang sangat lemah merupakan
14