Page 31 - E-MODUL_Neat
P. 31
-
b. Basa adalah zat yang jika dilarutkan dalam air melepaskan ion OH . Reaksi senyawa
basa di dalam air adalah sebagai berikut.
+
-
BOH (aq) B (aq) + OH (aq)
Salah satu contoh basa adalah amonia dengan rumus kimia NH 3. Jika NH 3 dilarutkan
-
dalam air maka akan terionisasi menjadi ion hidroksida (OH ) dan ion amonium
+
(NH 4 ).
Persamaan reaksinya sebagai berikut:
-
+
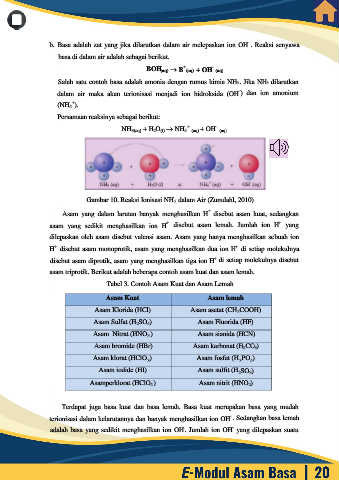
NH 3(aq) + H 2O (l) NH 4 (aq) + OH (aq)
Gambar 10. Reaksi Ionisasi NH 3 dalam Air (Zumdahl, 2010)
+
Asam yang dalam larutan banyak menghasilkan H disebut asam kuat, sedangkan
+
+
asam yang sedikit menghasilkan ion H disebut asam lemah. Jumlah ion H yang
dilepaskan oleh asam disebut valensi asam. Asam yang hanya menghasilkan sebuah ion
+
+
H disebut asam monoprotik, asam yang menghasilkan dua ion H di setiap molekulnya
+
disebut asam diprotik, asam yang menghasilkan tiga ion H di setiap molekulnya disebut
asam triprotik. Berikut adalah beberapa contoh asam kuat dan asam lemah.
Tabel 3. Contoh Asam Kuat dan Asam Lemah
Asam Kuat Asam lemah
Asam Klorida (HCl) Asam asetat (CH 3COOH)
Asam Sulfat (H 2SO 4) Asam Fluorida (HF)
Asam Nitrat (HNO 3) Asam sianida (HCN)
Asam bromide (HBr) Asam karbonat (H 2CO 3)
Asam klorat (HClO 3) Asam fosfat (H 3PO 4)
Asam iodide (HI) Asam sulfit (H 2SO 3)
Asamperklorat (HClO 4) Asam nitrit (HNO 2)
Terdapat juga basa kuat dan basa lemah. Basa kuat merupakan basa yang mudah
-
terionisasi dalam kelarutannya dan banyak menghasilkan ion OH . Sedangkan basa lemah
-
-
adalah basa yang sedikit menghasilkan ion OH . Jumlah ion OH yang dilepaskan suatu