Page 32 - E-modul Kimia Asam Basa
P. 32
Kesetimbangan Ion dalam Larutan
Asam Basa
Berdasarkan sifat asam basanya, larutan dikelompokkan menjadi
asam kuat, asam lemah, basa kuat dan basa lemah. Asam kuat dan
basa kuat mengalami ionisasi sempurna (α = 1).
mol zat yang terionisasi
α =
mol zat mula-mula
Adapun asam lemah dan basa lemah mengalami ionisasi sebagian
(0 < a < 1). Banyaknya zat yang mengalami ionisasi dinyatakan
dengan derajat ionisasi. Perbedaan ionisasi asam kuat dan asam
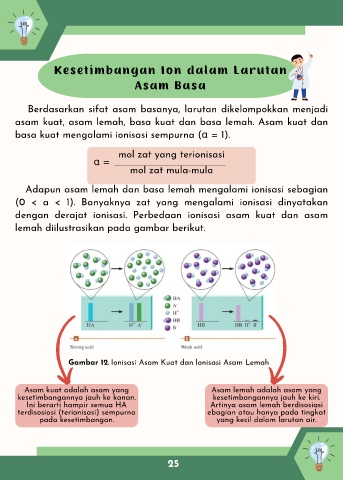
lemah diilustrasikan pada gambar berikut.
Gambar 12. Ionisasi Asam Kuat dan lonisasi Asam Lemah
Asam kuat adalah asam yang Asam lemah adalah asam yang
kesetimbangannya jauh ke kanan. kesetimbangannya jauh ke kiri.
Ini berarti hampir semua HA Artinya asam lemah berdisosiasi
terdisosiasi (terionisasi) sempurna ebagian atau hanya pada tingkat
pada kesetimbangan. yang kecil dalam larutan air.
25