Page 35 - E-modul Kimia Asam Basa
P. 35
Secara matematis, konsentrasi ion H⁺ untuk asam lemah dirumuskan:
√
[H⁺] = M × a [H⁺] = M × Ka
Keterangan:
Ka = Tetapan ionisasi asam
M = Konsentrasi larutan asam
a = Valensi asam
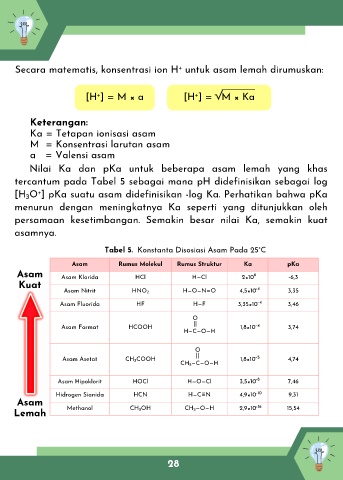
Nilai Ka dan pKa untuk beberapa asam lemah yang khas
tercantum pada Tabel 5 sebagai mana pH didefinisikan sebagai log
[H₃O⁺] pKa suatu asam didefinisikan -log Ka. Perhatikan bahwa pKa
menurun dengan meningkatnya Ka seperti yang ditunjukkan oleh
persamaan kesetimbangan. Semakin besar nilai Ka, semakin kuat
asamnya.
Tabel 5. Konstanta Disosiasi Asam Pada 25°C
Asam Rumus Molekul Rumus Struktur Ka pKa
Asam Asam Klorida HCl H—Cl 2×10 6 -6,3
Kuat
Asam Nitrit HNO₂ H—O—N=O 4,5×10 –4 3,35
Asam Fluorida HF H—F 3,35×10 –4 3,46
O
||
Asam Format HCOOH 1,8×10 –4 3,74
H—C—O—H
O
||
Asam Asetat CH₃COOH 1,8×10 –5 4,74
CH₃—C—O—H
Asam Hipoklorit HOCl H—O—Cl 3,5×10 –8 7,46
—
Hidrogen Sianida HCN H—C=N 4,9×10 –10 9,31
Asam
Methanol CH₃OH CH₃—O—H 2,9×10 –16 15,54
Lemah
28