Page 33 - E-modul Kimia Asam Basa
P. 33
Asam Kuat
Beberapa contoh asam kuat HCl, HBr, HI, H₂SO₄, HNO₃, HCIO₃,
HCIO₄, asam kuat mengalami ionisasi sempurna. Secara umum, jika
suatu asam kuat dilarutkan dalam air, maka reaksi yang terjadi
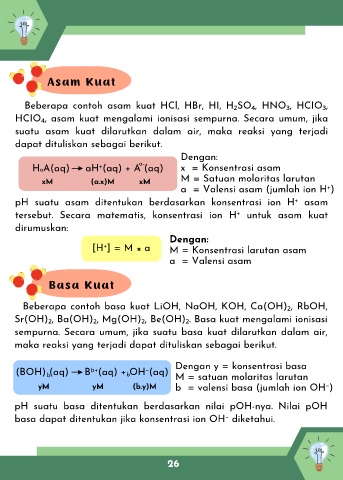
dapat dituliskan sebagai berikut.
Dengan:
a–
H A(aq) aH⁺(aq) + A (aq) x = Konsentrasi asam
a
M = Satuan molaritas larutan
xM (a.x)M xM
a = Valensi asam (jumlah ion H⁺)
pH suatu asam ditentukan berdasarkan konsentrasi ion H⁺ asam
tersebut. Secara matematis, konsentrasi ion H⁺ untuk asam kuat
dirumuskan:
Dengan:
[H⁺] = M × a M = Konsentrasi larutan asam
a = Valensi asam
Basa Kuat
Beberapa contoh basa kuat LiOH, NaOH, KOH, Ca(OH)₂, RbOH,
Sr(OH)₂, Ba(OH)₂, Mg(OH)₂, Be(OH)₂. Basa kuat mengalami ionisasi
sempurna. Secara umum, jika suatu basa kuat dilarutkan dalam air,
maka reaksi yang terjadi dapat dituliskan sebagai berikut.
Dengan y = konsentrasi basa
(BOH) (aq) Bᵇ⁺(aq) + OH⁻(aq) M = satuan molaritas larutan
b
b
yM yM (b.y)M b = valensi basa (jumlah ion OH⁻)
pH suatu basa ditentukan berdasarkan nilai pOH-nya. Nilai pOH
basa dapat ditentukan jika konsentrasi ion OH⁻ diketahui.
26