Page 22 - E-Modul Sifat Koligatif Larutan Berbasis SETS new
P. 22
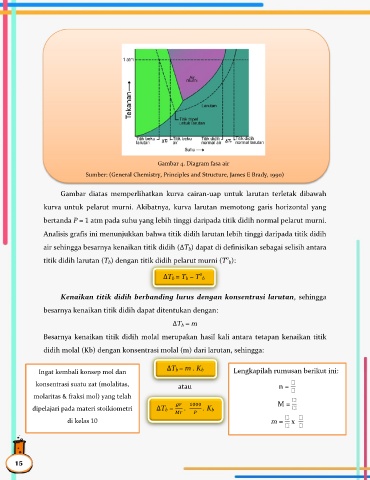
Gambar 4. Diagram fasa air
Sumber: (General Chemistry, Principles and Structure, James E Brady, 1990)
Gambar diatas memperlihatkan kurva cairan-uap untuk larutan terletak dibawah
kurva untuk pelarut murni. Akibatnya, kurva larutan memotong garis horizontal yang
bertanda P = 1 atm pada suhu yang lebih tinggi daripada titik didih normal pelarut murni.
Analisis grafis ini menunjukkan bahwa titik didih larutan lebih tinggi daripada titik didih
air sehingga besarnya kenaikan titik didih (∆T b) dapat di definisikan sebagai selisih antara
o
titik didih larutan (T b) dengan titik didih pelarut murni (T b):
o
∆T b = T b – T b
Kenaikan titik didih berbanding lurus dengan konsentrasi larutan, sehingga
besarnya kenaikan titik didih dapat ditentukan dengan:
∆T b = m
Besarnya kenaikan titik didih molal merupakan hasil kali antara tetapan kenaikan titik
didih molal (Kb) dengan konsentrasi molal (m) dari larutan, sehingga:
Ingat kembali konsep mol dan ∆T b = m . K b Lengkapilah rumusan berikut ini:
⬚
konsentrasi suatu zat (molalitas, atau n =
⬚
molaritas & fraksi mol) yang telah
⬚
1000 M =
dipelajari pada materi stoikiometri ∆T b = . . K b ⬚
⬚ ⬚
di kelas 10 m = x
⬚ ⬚
15