Page 11 - E-Modul Fisling Lidia Nia FIX_Neat
P. 11
Panas yang diterima oleh gas digunakan untuk dua hal, yaitu untuk menaikkan energi
dan untuk melakukan usaha luar.
Q = ΔU + W (1.9) M
Q = panas yang diterima oleh gas
ΔU = perubahan energi dalam gas
W = usaha yang dilakukan oleh gas
Dari persamaan di atas diperoleh:
Q = positif jika gas (sistem) menerima panas
Q = negatif jika gas (sistem) memberikan panas
ΔU = positif jika energi dalam gas (sistem) bertambah
ΔU = negatif jika energi dalam gas (sistem) berkurang
W = positif jika gas (sistem) melakukan usaha (kerja)
W = negatif jika gas (sistem) menerima usaha (kerja)
3) Proses dalam Termodinamika
Usaha yang terdapat pada gas yang mengalami proses-proses termodinamika tersebut
akan diuraikan sebagai berikut.
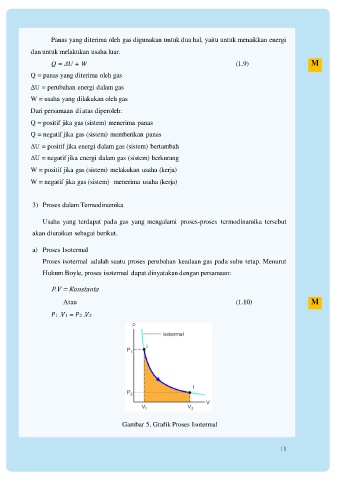
a) Proses Isotermal
Proses isotermal adalah suatu proses perubahan keadaan gas pada suhu tetap. Menurut
Hukum Boyle, proses isotermal dapat dinyatakan dengan persamaan:
P.V = Konstanta
Atau (1.10) M
1 . 1 = 2 . 2
Gambar 5. Grafik Proses Isotermal
11