Page 682 - Traité de Chimie Thérapeutique 4 Médicaments en relation avec des systèmes hormonaux
P. 682
16. VITAMINES D HTDÉRIVÉS 643
- l'électronégativité du fluor peut provoquer des modifications conformationnelles
lors d'une interaction avec un site de liaison.
7.1.3.1. FLUORATION EN 1,3 OU 25
Le remplacement de l'hydroxyle en 25 du calcitriol par un fluor conduit à la 25-F-1a-
OH-D3 qui est très nettement moins active que ce dernier au niveau de la fixation sur
la DBP. Mais, la 25-F-24fî-OH-D3 qui présente, elle aussi, une très faible affinité in
vitro, possède in vivo une activité analogue à celle de la 25-OH-D3. Ceci est probable
ment dû à une hydroxylation en 1a par le rein conduisant à la 25-F-1a,24-(OH)2-D3.
Ceci montre que l'hydroxylation en 25 n'est pas une voie obligatoire de l'activité
endocrine de la vitamine D et que la présence d’un hydroxyle en 24 peut, dans ce cas,
suppléer l'hydroxyle en 25 (Napoli et al.).
Le remplacement en 1 conduit à la 1a-F-D3 et à la 1 a-F-25-OH-D3. Cette dernière
se lie à la DBP avec une affinité supérieure à celle du calcitriol, mais s’avère moins
active dans le transfert intestinal du calcium et sa mobilisation à partir de l'os.
La 1a,25-F2-D3 est totalement inactive, la présence des atomes de fluor empê
chant les deux hydroxylations de se produire.
Le remplacement en 30 conduit à la 3p-F-D3 qui ne possède pas d'activité vitami
nique D in vitro. Par contre, la 3p-F-1a-OH-D3 induit la formation de CaBP et stimule
l’absorption intestinale du calcium.
OH
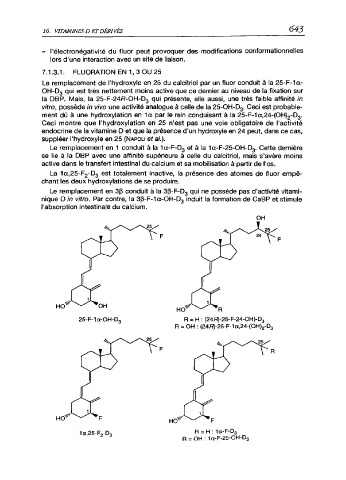
25-F-1a-OH-D3 R = H : (24H)-25-F-24-OH)-D3
R = OH : (24H)-25-F-1a,24-(OH)2-D3
1a,25-F2-D3 R = H : 1a-F-D3
R = OH : 1a-F-25-OH-D3