Page 18 - Salinan dari Salinan dari E-Modul Asam Basa (220 x 297 mm) (220 x 307 mm)
P. 18
TEORI ASAM BASA
memiliki pasangan elektron yang dapat digunakan secara bersama.
Maka rekasi asam basa menurut Lewis berkaitan dengan transfer.
pasangan elektron sehingga terbentuk ikatan kovalen koordinasi..
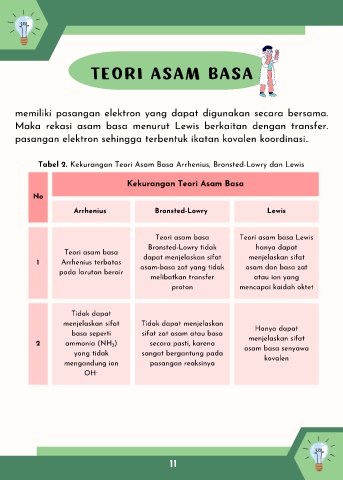
Tabel 2. Kekurangan Teori Asam Basa Arrhenius, Bronsted-Lowry dan Lewis
Kekurangan Teori Asam Basa
No
Arrhenius Bronsted-Lowry Lewis
Teori asam basa Teori asam basa Lewis
Bronsted-Lowry tidak hanya dapat
Teori asam basa
dapat menjelaskan sifat menjelaskan sifat
1 Arrhenius terbatas
asam-basa zat yang tidak asam dan basa zat
pada larutan berair
melibatkan transfer atau ion yang
proton mencapai kaidah oktet
Tidak dapat
menjelaskan sifat Tidak dapat menjelaskan
Hanya dapat
basa seperti sifat zat asam atau basa
menjelaskan sifat
2 ammonia (NH₃) secara pasti, karena
asam basa senyawa
yang tidak sangat bergantung pada
kovalen
mengandung ion pasangan reaksinya
OH⁻
11