Page 13 - 00_sampul_depan.pdf
P. 13
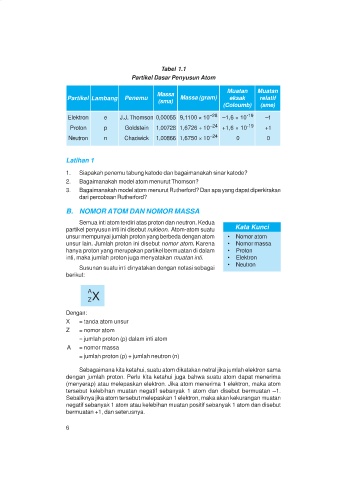
Tabel 1.1
Partikel Dasar Penyusun Atom
Muatan Muatan
Massa
Partikel Lambang Penemu Massa (gram) eksak relatif
(sma)
(Coloumb) (sme)
Elektron e J.J. Thomson 0,00055 9,1100 × 10 –28 –1,6 × 10 -19 –1
Proton p Goldstein 1,00728 1,6726 + 10 –24 +1,6 × 10 -19 +1
Neutron n Chadwick 1,00866 1,6750 × 10 –24 0 0
Latihan 1
1. Siapakah penemu tabung katode dan bagaimanakah sinar katode?
2. Bagaimanakah model atom menurut Thomson?
3. Bagaimanakah model atom menurut Rutherford? Dan apa yang dapat diperkirakan
dari percobaan Rutherford?
B. NOMOR ATOM DAN NOMOR MASSA
Semua inti atom terdiri atas proton dan neutron. Kedua
partikel penyusun inti ini disebut nukleon. Atom-atom suatu Kata Kunci
unsur mempunyai jumlah proton yang berbeda dengan atom • Nomor atom
unsur lain. Jumlah proton ini disebut nomor atom. Karena • Nomor massa
hanya proton yang merupakan partikel bermuatan di dalam • Proton
inti, maka jumlah proton juga menyatakan muatan inti. • Elektron
• Neutron
Susunan suatu inti dinyatakan dengan notasi sebagai
berikut:
A
Z X
Dengan:
X = tanda atom unsur
Z = nomor atom
= jumlah proton (p) dalam inti atom
A = nomor massa
= jumlah proton (p) + jumlah neutron (n)
Sebagaimana kita ketahui, suatu atom dikatakan netral jika jumlah elektron sama
dengan jumlah proton. Perlu kita ketahui juga bahwa suatu atom dapat menerima
(menyerap) atau melepaskan elektron. Jika atom menerima 1 elektron, maka atom
tersebut kelebihan muatan negatif sebanyak 1 atom dan disebut bermuatan –1.
Sebaliknya jika atom tersebut melepaskan 1 elektron, maka akan kekurangan muatan
negatif sebanyak 1 atom atau kelebihan muatan positif sebanyak 1 atom dan disebut
bermuatan +1, dan seterusnya.
6