Page 101 - BUKU KIMIA KELAS XI PJBL
P. 101
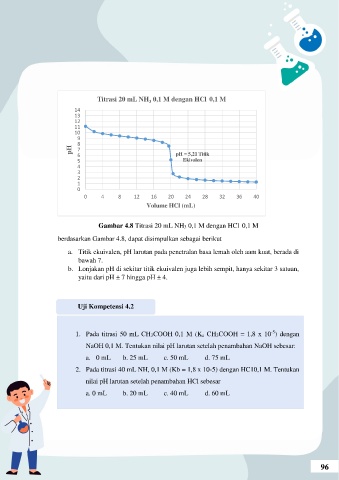
Titrasi 20 mL NH 0,1 M dengan HCl 0,1 M
3
14
13
12
11
10
9
8
pH 7
6 pH = 5,21 Titik
5 Ekivalen
4
3
2
1
0
0 4 8 12 16 20 24 28 32 36 40
Volume HCl (mL)
Gambar 4.8 Titrasi 20 mL NH3 0,1 M dengan HCl 0,1 M
berdasarkan Gambar 4.8, dapat disimpulkan sebagai berikut
a. Titik ekuivalen, pH larutan pada penetralan basa lemah oleh aam kuat, berada di
bawah 7.
b. Lonjakan pH di sekitar titik ekuivalen juga lebih sempit, hanya sekitar 3 satuan,
yaitu dari pH ± 7 hingga pH ± 4.
Uji Kompetensi 4.2
-5
1. Pada titrasi 50 mL CH3COOH 0,1 M (Ka CH3COOH = 1,8 x 10 ) dengan
NaOH 0,1 M. Tentukan nilai pH larutan setelah penambahan NaOH sebesar:
a. 0 mL b. 25 mL c. 50 mL d. 75 mL
2. Pada titrasi 40 mL NH, 0,1 M (Kb = 1,8 x 10-5) dengan HC10,1 M. Tentukan
nilai pH larutan setelah penambahan HCl sebesar
a. 0 mL b. 20 mL c. 40 mL d. 60 mL
96
7