Page 1064 - medicina-integrativa_compress
P. 1064
CAPÍTULO 105 PRESCRIPCIÓN DE FITOFÁRMACOS 1093
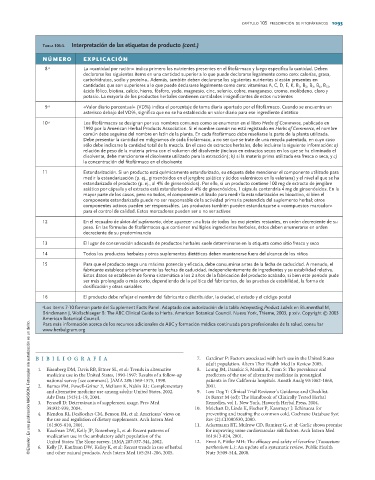
Tabla 105-5. Interpretación de las etiquetas de producto (cont.)
NÚMERO EXPLICACIÓN
a
8 La «cantidad por ración» indica primero los nutrientes presentes en el fitofármaco y luego especifica la cantidad. Deben
declararse los siguientes ítems en una cantidad superior a lo que puede declararse legalmente como cero: calorías, grasa,
carbohidratos, sodio y proteína.. Además, también deben declararse los siguientes nutrientes si están presentes en
cantidades que son superiores a lo que puede declararse legalmente como cero: vitaminas A, C, D, E, K, B 1 , B 2 , B 3 , B 6 , B 12 ,
ácido fólico, biotina, calcio, hierro, fósforo, yodo, magnesio, cinc, selenio, cobre, manganeso, cromo, molibdeno, cloro y
potasio. La mayoría de los productos herbales contienen cantidades insignificantes de estos nutrientes
a
9 «Valor diario porcentual» (VD%) indica el porcentaje de toma diaria aportado por el fitofármaco. Cuando se encuentra un
asterisco debajo del VD%, significa que no se ha establecido un valor diario para ese ingrediente dietético
a
10 Los fitofármacos se designan por sus nombres comunes como se enumeran en el libro Herbs of Commerce, publicado en
1992 por la American Herbal Products Association. Si el nombre común no está registrado en Herbs of Commerce, el nombre
común debe seguirse del nombre en latín de la planta. En cada fitofármaco debe reseñarse la parte de la planta utilizada.
Debe presentar la cantidad en miligramos de cada fitofármaco, a no ser que se trate de una mezcla patentada, en cuyo caso
sólo debe indicarse la cantidad total de la mezcla. En el caso de extractos herbales, debe incluirse la siguiente información: a)
relación de peso de la materia prima con el volumen del disolvente (incluso en extractos secos en los que se ha eliminado el
disolvente, debe mencionarse el disolvente utilizado para la extracción); b) si la materia prima utilizada era fresca o seca, y c)
la concentración del fitofármaco en el disolvente
11 Estandarización. Si un producto está químicamente estandarizado, su etiqueta debe mencionar el componente utilizado para
medir la estandarización (p. ej., ginsenósidos en el jengibre asiático y ácidos valerénicos en la valeriana) y el nivel al que se ha
estandarizado el producto (p. ej., al 4% de ginsenósidos). Por ello, si un producto contiene 100 mg de extracto de jengibre
asiático por cápsula y el extracto está estandarizado al 4% de ginsenósidos, 1 cápsula contendría 4 mg de ginsenósidos. En la
mayor parte de los casos, pero no todos, el componente utilizado para medir la estandarización es bioactivo, si bien el
componente estandarizado puede no ser responsable de la actividad primaria pretendida del suplemento herbal; otros
componentes activos pueden ser responsables. Los productos también pueden estandarizarse a «compuestos marcador»
para el control de calidad. Estos marcadores pueden ser o no ser activos
12 En el recuadro de datos del suplemento, debe aparecer una lista de todos los excipientes restantes, en orden decreciente de su
peso. En las fórmulas de fitofármacos que contienen múltiples ingredientes herbales, éstos deben enumerarse en orden
decreciente de su predominancia
13 El lugar de conservación adecuada de productos herbales suele determinarse en la etiqueta como sitio fresco y seco
14 Todos los productos herbales y otros suplementos dietéticos deben mantenerse fuera del alcance de los niños
15 Para que el producto tenga una máxima potencia y eficacia, debe consumirse antes de la fecha de caducidad. A menudo, el
fabricante establece arbitrariamente las fechas de caducidad, independientemente de ingredientes y su estabilidad relativa.
Estos datos se establecen de forma sistemática a los 2 años de la fabricación del producto acabado, si bien este período pude
ser más prolongado o más corto, dependiendo de la política del fabricantes, de las pruebas de estabilidad, la forma de
dosificación y otras variables
16 El producto debe reflejar el nombre del fabricante o distribuidor, la ciudad, el estado y el código postal
a Los items 7-10 forman parte del Supplement Facts Panel. Adaptado con autorización de la tabla Interpreting Product Labels en Blumenthal M,
Brinckmann J, Wollschlaeger B: The ABC Clinical Guide to Herbs. American Botanical Council. Nueva York, Thieme, 2003, p xxiv. Copyright © 2003
American Botanical Council.
© Elsevier. Es una publicación MASSON. Fotocopiar sin autorización es un delito.
Para más información acerca de los recursos adicionales de ABC y formación médica continuada para profesionales de la salud, consultar
www.herbalgram.org
BIBILIOGRAFÍA 7. Gardiner P: Factors associated with herb use in the United States
adult population. Altern Ther Health Med In Review 2005.
1. Eisenberg DM, Davis RB, Ettner SL, et al: Trends in alternative 8. Leung JM, Dzankic S, Manku K, Yuan S: The prevalence and
medicine use in the United States, 1990-1997: Results of a follow-up predictors of the use of alternative medicine in presurgical
national survey [see comment]. JAMA 280:1569-1575, 1998. patients in five California hospitals. Anesth Analg 93:1062-1068,
2. Barnes PM, Powell-Griner E, McFann K, Nahin RL: Complementary 2001.
and alternative medicine use among adults: United States, 2002. 9. Low Dog T: Clinical Trial Reviewer’s Guidance and Checklist.
Adv Data (343):1-19, 2004. In Barret M (ed): The Handbook of Clinically Tested Herbal
3. Fennell D: Determinants of supplement usage. Prev Med Remedies, vol 1. New York, Haworth Herbal Press, 2004.
39:932-939, 2004. 10. Melchart D, Linde K, Fischer P, Kaesmayr J: Echinacea for
4. Blendon RJ, DesRoches CM, Benson JM, et al: Americans’ views on preventing and treating the common cold. Cochrane Database Syst
the use and regulation of dietary supplements. Arch Intern Med Rev (2):CD000530, 2000.
161:805-810, 2001. 11. Ackermann RT, Mulrow CD, Ramirez G, et al: Garlic shows promise
5. Kaufman DW, Kelly JP, Rosenberg L, et al: Recent patterns of for improving some cardiovascular risk factors. Arch Intern Med
medication use in the ambulatory adult population of the 161:813-824, 2001.
United States: The Slone survey. JAMA 287:337-344, 2002. 12. Ernst E, Pittler MH: The efficacy and safety of feverfew (Tanacetum
6. Kelly JP, Kaufman DW, Kelley K, et al: Recent trends in use of herbal parthenium L.): An update of a systematic review. Public Health
and other natural products. Arch Intern Med 165:281-286, 2005. Nutr 3:509-514, 2000.