Page 173 - Traité de Chimie Thérapeutique 2 : Médicaments Antibiotiques
P. 173
163
3. LES CÉPHALOSPORINES
Dans ce but, l'isopropylidène-acétate est transformé en triphénylphosphory-
lidène-acétate en quatre étapes :
1 - ozonolyse ;
2 - réduction régiospécifique du carbonyle par le couple Zn/CH,COOH;
3- transformation de l'alcool en chlorure ;
4- passage au sel de phosphionum puis à l'ylure de phosphore en milieu basi-
que ( réactif de Wittig) VII 1.
La réaction de Wittig intramoléculaire conduit à l'1-oxacéphème DX. La fonc-
tion aminée en 7 est ensuite libérée afin d'introduire le méthoxyle en 7 a. Cette
opération nécessite, comme nous l'avons vu précédemment, trois étapes (X).
3• temps : Introduction du méthoxyle 7 a ( cf. céphamycines)
- formation d'une imine par condensation avec le 3,5-di-tert-butyl
4-hydroxybenzaldéhyde DBHD ;
oxydation par le peroxyde de nickel en un intermédiaire pseudoquinonique ;
addition de méthanol sur la quinone-imine ;
- obtention du 7[-amino-7 a-méthoxy-A-céphème XI à l'aide du réactif T de
Girard.
4 temps : Acylation de l'amlne en 7
Le 1-oxacéphème est acylé dans les conditions habituelles par l'hémichlorure
de l'acide 4-hydroxyphénylmalonique convenablement protégé. L'élimination des
groupements protecteurs est réalisée par traitement CF COOH/anisole ou
3
AICI3/anisole.
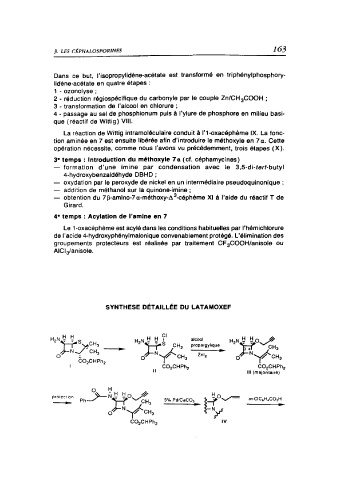
SYNTHESE DÉTAILLÉE DU LATAMOXEF
alcool
propargyltque
zl,
--- 5% Pd/CaCO,
protection