Page 226 - Traité de Chimie Thérapeutique 2 : Médicaments Antibiotiques
P. 226
216 MÉDICAMENTS ANTIBIOTIQUES
2.4. APPLICATION : SYNTHÈSE DE L'AZTRÉONAM
Elle comprend schématiquement trois étapes:
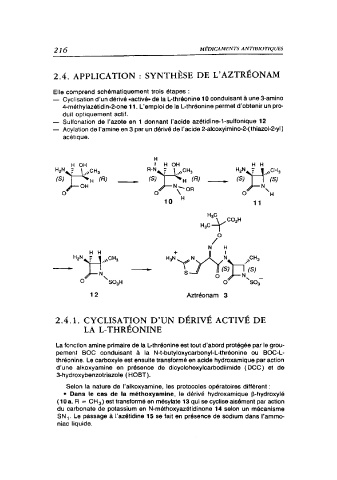
- Cyclisation d'un dérivé «activé» de la L-thréonine 10 conduisant à une 3-amino
4-méthylazétidin-2-one 11. L'emploi de la L-thréonine permet d'obtenir un pro-
duit optiquement actif.
Sulfonation de l'azote en 1 donnant l'acide azétidine-1-sulfonique 12
Acylation de l'amine en 3 par un dérivé de l'acide 2-alcoxyimino-2-(thiazol-2-yl)
acétique.
H
::
1 H OH
- R-N)=:;,CH3 » -
s»'
0 N- op
\
10 H
12 Aztréonam 3
2.4.1. CYCLISATION D'UN DÉRIVÉ ACTIVÉ DE
LA L-THRÉONINE
La fonction amine primaire de la L-thréonine est tout d'abord protégée par le grou-
pement BOC conduisant à la N-t-butyloxycarbonyl-L-thréonine ou BOC-L-
thréonine. Le carboxyle est ensuite transformé en acide hydroxamique par action
d'une alkoxyamine en présence de dicyclohexylcarbodiimide ( DCC) et de
3-hydroxybenzotriazole ( HOBT).
Selon la nature de l'alkoxyamine, les protocoles opératoires diffèrent :
• Dans le cas de la méthoxyamlne, le dérivé hydroxamique P-hydroxylé
(10a, R = CH,) est transformé en mésylate 13 qui se cyclise aisément par action
du carbonate de potassium en N-méthoxyazétidinone 14 selon un mécanisme
SN,.Le passage à l'azétidine 15 se fait en présence de sodium dans l'ammo-
niac liquide.