Page 228 - Traité de Chimie Thérapeutique 2 : Médicaments Antibiotiques
P. 228
218 MÉDICAMENTS ANTIBIOTIQUES
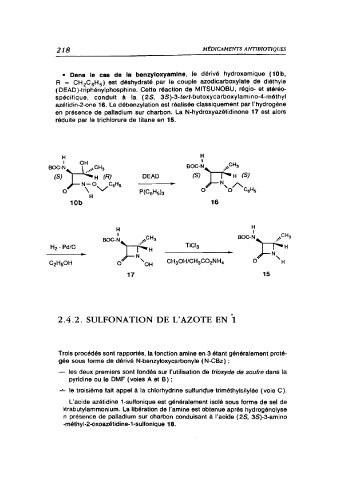
• Dans le cas de la benzyloxyamlne, le dérivé hydroxamique (10b,
A = CH C H ) est déshydraté par le couple azodicarboxylate de diéthyle
2 6 5
( OEAD )-triphénylphosphine. Cette réaction de MITSUNOBU, régio- et stéréo-
spécifique, conduit à la ( 2S, 3S)-3-tert-butoxycarboxylamino-4-méthyl
azétidin-2-one 16. La débenzylation est réalisée classiquement par l'hydrogène
en présence de palladium sur charbon. La N-hydroxyazétidinone 17 est alors
réduite par le trichlorure de titane en 15.
H
1 OH
BOC-N):::CH3
,
·•'
(S) H (R) OEAD
N-O CaH;
0 \ '-../
H
10b 16
H
1 CH,
,:.
BOC-N'i--f H
/.
0
17 15
2.4.2. SULFONATION DE L'AZOTE EN ·1
Trois procédés sont rapportés, la fonction amine en 3 étant généralement proté-
gée sous forme de drivé N-benzyloxycarbonyle (N-CBz):
- les deux premiers sont fondés sur l'utilisation de trioxyde de soufre dans la
pyridine ou le DMF (voies A et B);
..,_ le troisième fait appel à la chlorhydrine sulfurique triméthylsilylée (voie C).
L'acide azétidine 1-sulfonique est généralement isolé sous forme de sel de
trabutylammonium. La libération de l'amine est obtenue après hydrogénolyse
n présence de palladium sur charbon conduisant à l'acide (2S, 3S)-3-amino
-méthyl-2-oxoazétidine-1-sulfonique 18.