Page 54 - Chimie organique - cours de Pau 2- Brigitte Jamart
P. 54
Chapitre 2 ■ La géométrie des molécules organiques
E
·~· ! 3,8 kJ.mol- 1
--------------------------------------------------------
CH, CH,
c/[n1 1/[5c1,
1
H H
Degré de rotation
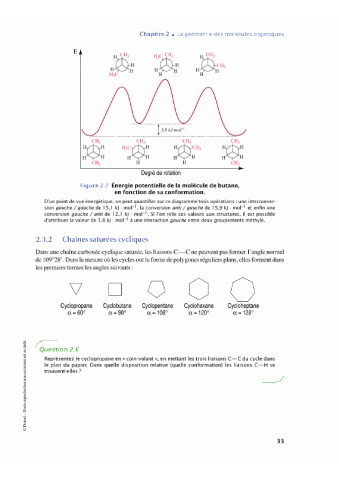
Figure 2.7 Énergie potentielle de la molécule de butane,
en fonction de sa conformation.
D'un point de vue énergétique, on peut quantifier sur ce diagramme trois opérations: une interconver-
1
sion gauche/gauche de l 5, l kJ· mol', la conversion anti /gauche de l 5,9 kJ • moi- et enfin une
1
conversion gauche / anti de 12, l kJ • moi- • Si l'on relie ces valeurs aux structures, il est possible
1
d'attribuer la valeur de 3,8 kJ • moi- à une interaction gauche entre deux groupements méthyle.
2.3.2 Chaînes saturées cycliques
Dans une chaîne carbonée cyclique saturée, les liaisons C-C ne peuvent pas former l'angle normal
de 109°28'. Dans la mesure où les cycles ont la forme de polygones réguliers plans, elles forment dans
les premiers termes les angles suivants :
7 □ 0 C 0
Cyclopropane Cyclobutane Cyclopentane Cyclohexane Cycloheptane
a= 60° 0. = 90° a= 108° a= 120° a= 128°
'auesion2.E
Représentez le cyclopropane en « coin-volant », en mettant les trois liaisons CC du cycle dans
le plan du papier. Dans quelle disposition relative (quelle conformation) les liaisons CH se
trouvent-elles?
33