Page 75 - Majalah PERHAPI Edisi 007 Juli-September 2021
P. 75
PAPER
[15]
(EW) . Larutan dari hasil pelindian selanjutnya dila- Pada ekstraksi pelarut tembaga dengan Mex-
kukan esktrasi pelarut untuk meningkatkan kadar tral 5640H melibatkan reaksi pembentukan senyawa
logam yang ingin diambil (recovery ) dan untuk me- melalui pertukaran kation, reaksi nya sebagai be-
ngurangi kadar pengotor dalam larutan. Hal ini dila- rikut :
+
kukan agar proses selanjutnya yaitu electrowinning 2RH (org) + Cu 2+ (aq) → R Cu (org) + 2H (aq)
2
dapat berjalan efesien. Ekstraksi pelarut biasanya dimana R merupakan bentuk umum dari senyawa
dilakukan dengan ekstraktan berupa larutan organik organik dalam ekstraktan .
[17]
[16]
. Ekstraktan organik tembaga yang banyak digu- Setelah dilakukan ekstraksi pelarut, dilakukan
nakan yaitu LIX 84-I, LIX 984N, Acorga M5640 dan stripping untuk mendapatkan larutan Cu dalam fasa
[17]
Mextral 5640H . aqeous kembali. Pada percobaan [17] juga dilakukan
Pada Percobaan [17] dilakukan ekstraksi pela- percobaan stripping yang dilakukan di dalam gelas
rut dari larutan yang kaya akan tembaga yang be- kimia berukuran 100 ml. Percobaan tersebut dilaku-
rasal dari limbah elektrolit pemurnian perak. Pada kan dengan mencampur larutan organik hasil eks-
percobaan tersebut, ekstraktan organik yang digu- trasi dengan larutan aqeous berupa CuSO dengan
4
nakan yaitu Mextral 5640H yang diencerkan dengan kadar Cu 35 gpl. Dilakukan juga pemanasan diatas
Escaid 110. Percobaan ekstraksi pelarut ini dilakukan hot plate dengan temperatur tertentu dan dilakukan
dalam gelas kimia berukuran 250 ml dan dilakukan pengadukan selama 20 menit. Proses pemisahan la-
pengadukan lalu dilakukan pengaturan pH dengan rutan dilakukan dengan corong pemisah. Hasil yang
menambahkan NaOH 10 M dan H SO 10 M hingga didapat yaitu persen recovery dari Cu sebesar 87%
4
2
pH-nya sesuai. setelah itu dilakukan pemanasan di- pada nisbah O/A 2/1, Temperatur 46 C dan konsen-
o
atas hot plate dan digunakan corong untuk pemisa- trasi asam sulfat 200 gpl. Reaksi kimia yang terjadi
han larutan fasa organik dan aqeous . Variabel yang proses stripping merupakan reaksi kebalikan dari
digunakan dalam percobaan ini yaitu pH, konsen- reaksi kimia pada proses ekstraksi pelarut. Ion tem-
trasi ekstraktan (v/v) dan nisbah O/A (perbandingan baga dari fase organik dilepaskan untuk menjadi fase
fasa organik dengan aqeous ). Hasil yang didapatkan aqeous kembali. Reaksi nya sebagai berikut :
yaitu ekstraksi tertinggi dari Cu yaitu 97% pada pH 2,
konsentrasi ekstraktan 25% (v/v) dan nisbah O/A- + + Cu 2+
2
R Cu (org) + 2H (aq) → 2RH (org) (aq)
[17]
nya 2/1 . R merupakan bentuk umum dari senyawa or-
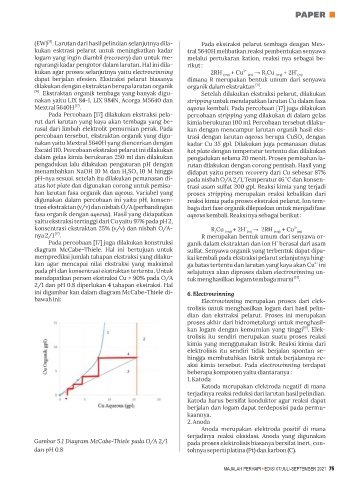
Pada percobaan [17] juga dilakukan konstruksi ganik dalam ekstraktan dan ion H berasal dari asam
+
diagram McCabe-Thiele. Hal ini bertujuan untuk sulfat. Senyawa organik yang terbentuk dapat dipa-
memprediksi jumlah tahapan ekstraksi yang dilaku- kai kembali pada ekstraksi pelarut selanjutnya hing-
kan agar mencapai nilai ekstraksi yang maksimal ga batas tertentu dan larutan yang kaya akan Cu ini
2+
pada pH dan konsentrasi ekstraktan tertentu. Untuk selajutnya akan diproses dalam electrowinning un-
mendapatkan persen ekstraksi Cu > 90% pada O/A tuk menghasilkan logam tembaga murni .
[17]
2/1 dan pH 0.8 diperlukan 4 tahapan ekstraksi. Hal
ini digambar kan dalam diagram McCabe-Thiele di-
6. Electrowinning
bawah ini: Electrowinning merupakan proses dari elek-
trolisis untuk menghasilkan logam dari hasil pelin-
dian dan ekstraksi pelarut. Proses ini merupakan
proses akhir dari hidrometalurgi untuk menghasil-
[18]
kan logam dengan kemurnian yang tinggi . Elek-
trolisis itu sendiri merupakan suatu proses reaksi
kimia yang menggunakan listrik. Reaksi kimia dari
elektrolisis itu sendiri tidak berjalan spontan se-
hingga membutuhkan listrik untuk berjalannya re-
aksi kimia tersebut. Pada electrowinning terdapat
beberapa komponen yaitu diantaranya :
1. Katoda
Katoda merupakan elektroda negatif di mana
terjadinya reaksi reduksi dari larutan hasil pelindian.
Katoda harus bersifat konduktor agar reaksi dapat
berjalan dan logam dapat terdeposisi pada permu-
kaannya.
2. Anoda
Anoda merupakan elektroda positif di mana
terjadinya reaksi oksidasi. Anoda yang digunakan
Gambar 5.1 Diagram McCabe-Thiele pada O/A 2/1 pada proses elektrolisis biasanya bersifat inert, con-
dan pH 0.8 tohnya seperti platina (Pt) dan karbon (C).
MAJALAH PERHAPI EDISI 07/JULI-SEPTEMBER 2021 75