Page 32 - Emodul Ayu Ningsih OK 23 juni 2025
P. 32
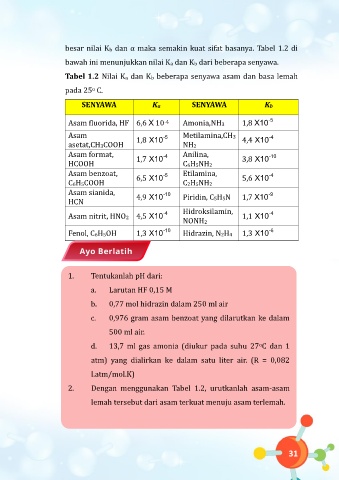
besar nilai Kb dan α maka semakin kuat sifat basanya. Tabel 1.2 di
bawah ini menunjukkan nilai Ka dan Kb dari beberapa senyawa.
Tabel 1.2 Nilai Ka dan Kb beberapa senyawa asam dan basa lemah
pada 25 C.
o
SENYAWA Ka SENYAWA Kb
-5
Asam fluorida, HF 6,6 X 10 Amonia,NH3 1,8 X10
-4
Asam 1,8 X10 Metilamina,CH3 4,4 X10
-4
-5
asetat,CH3COOH NH2
Asam format, -4 Anilina, -10
HCOOH 1,7 X10 C6H5NH2 3,8 X10
Asam benzoat, 6,5 X10 Etilamina, 5,6 X10
-4
-5
C6H5COOH C2H5NH2
Asam sianida, 4,9 X10 Piridin, C5H5N 1,7 X10
-10
-9
HCN
Hidroksilamin,
-4
-4
Asam nitrit, HNO2 4,5 X10 1,1 X10
NONH2
-10
-6
Fenol, C6H5OH 1,3 X10 Hidrazin, N2H4 1,3 X10
1. Tentukanlah pH dari:
a. Larutan HF 0,15 M
b. 0,77 mol hidrazin dalam 250 ml air
c. 0,976 gram asam benzoat yang dilarutkan ke dalam
500 ml air.
d. 13,7 ml gas amonia (diukur pada suhu 27 C dan 1
o
atm) yang dialirkan ke dalam satu liter air. (R = 0,082
l.atm/mol.K)
2. Dengan menggunakan Tabel 1.2, urutkanlah asam-asam
lemah tersebut dari asam terkuat menuju asam terlemah.
31